图1: MSWI飞灰预处理流程和超快碳热过程示意图
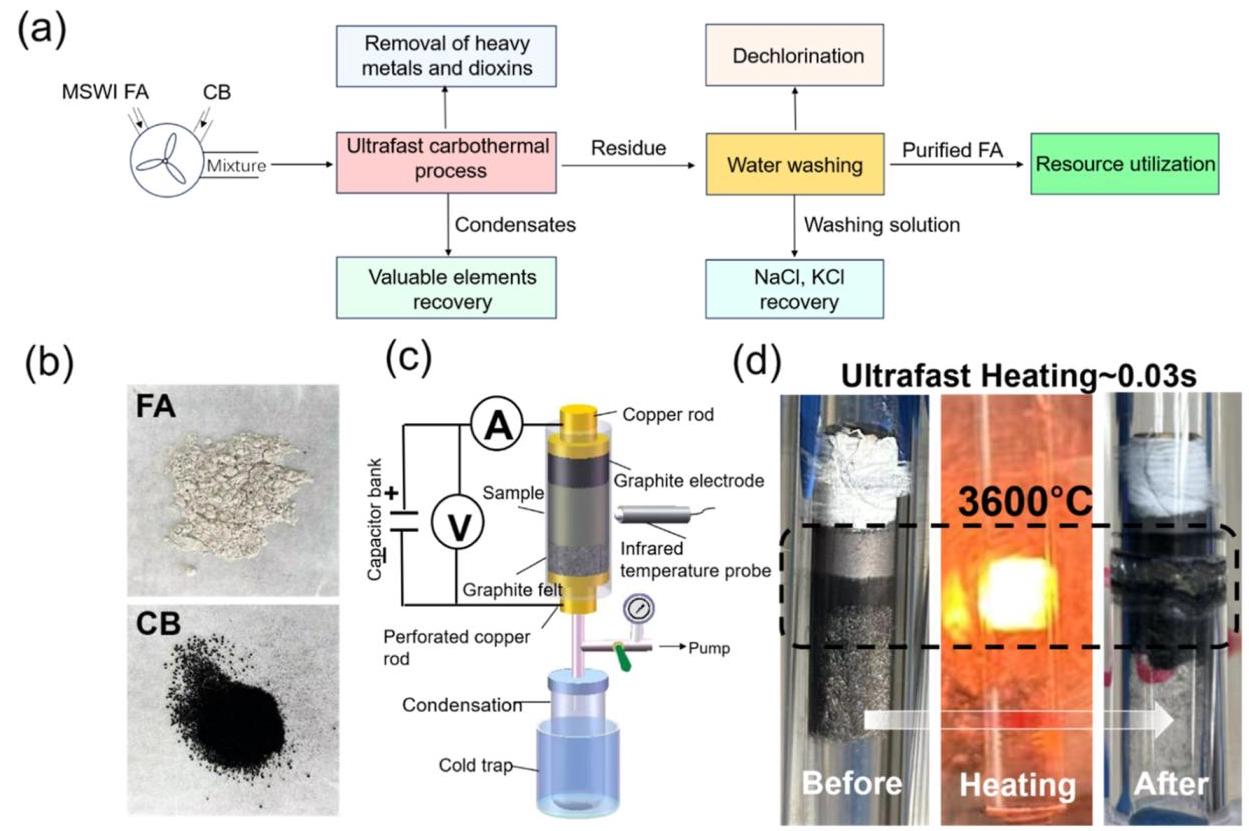
图1: (a) MSWI飞灰资源化利用预处理流程; (b) MSWI飞灰和导电炭黑的实物图; (c) 超快碳热过程反应器示意图; (d) 样品加热实物图
分析结果: 该图展示了完整的飞灰处理流程,从初始的飞灰-炭黑混合到超快加热过程,以及最终的产物收集。反应器设计允许在极短时间内实现高温处理,并通过冷阱有效收集挥发的有价值元素。
第一作者: Tengfei Zheng (南京师范大学)
通讯作者: Xinye Wang (南京师范大学), Haining Meng (光大环保技术装备(常州)有限公司)

图1: (a) MSWI飞灰资源化利用预处理流程; (b) MSWI飞灰和导电炭黑的实物图; (c) 超快碳热过程反应器示意图; (d) 样品加热实物图
分析结果: 该图展示了完整的飞灰处理流程,从初始的飞灰-炭黑混合到超快加热过程,以及最终的产物收集。反应器设计允许在极短时间内实现高温处理,并通过冷阱有效收集挥发的有价值元素。
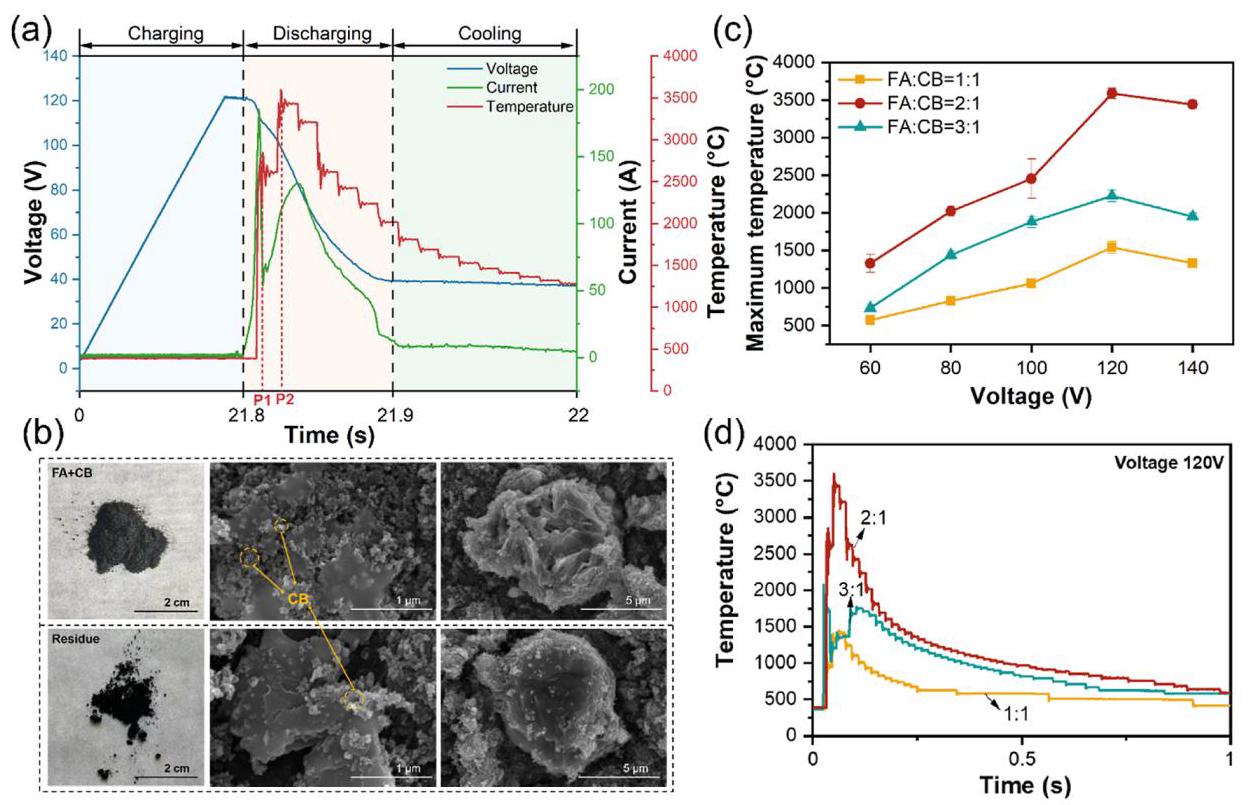
图2: (a) 超快碳热过程中电压、电流和温度随时间的变化(FA/CB=2:1, 初始电压120V); (b) 超快碳热过程前后样品的SEM图像; (c) 三种质量比和五种初始电压下的最高温度; (d) 整个加热阶段三种质量比在120V初始电压下的温度变化
分析结果: 超快加热过程显示出两个明显的温度峰值,第一个峰值在0.006秒达到约2700°C,第二个峰值在0.03秒达到约3600°C。SEM图像显示处理后飞灰颗粒表面仅有轻微熔化,无显著烧结现象,表明超快加热避免了传统热处理中的完全熔化问题。
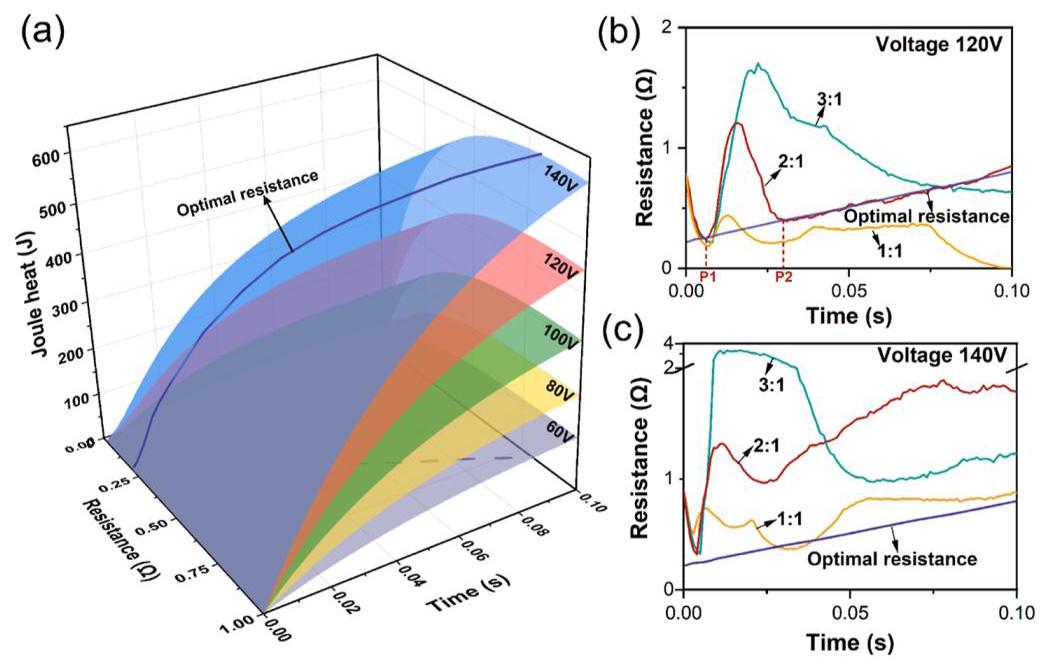
图3: (a) 五种初始电压下样品累积热量和电阻随时间变化的理论计算; (b) 120V和(c) 140V下实际样品电阻和理论最优电阻随时间变化
分析结果: 理论计算显示存在一个最优电阻值可使加热效果最大化。FA/CB质量比为2:1时,实际电阻最接近理论最优值,因此加热效果最好。140V电压下样品电阻偏离最优值更远,导致加热效果反而不如120V。
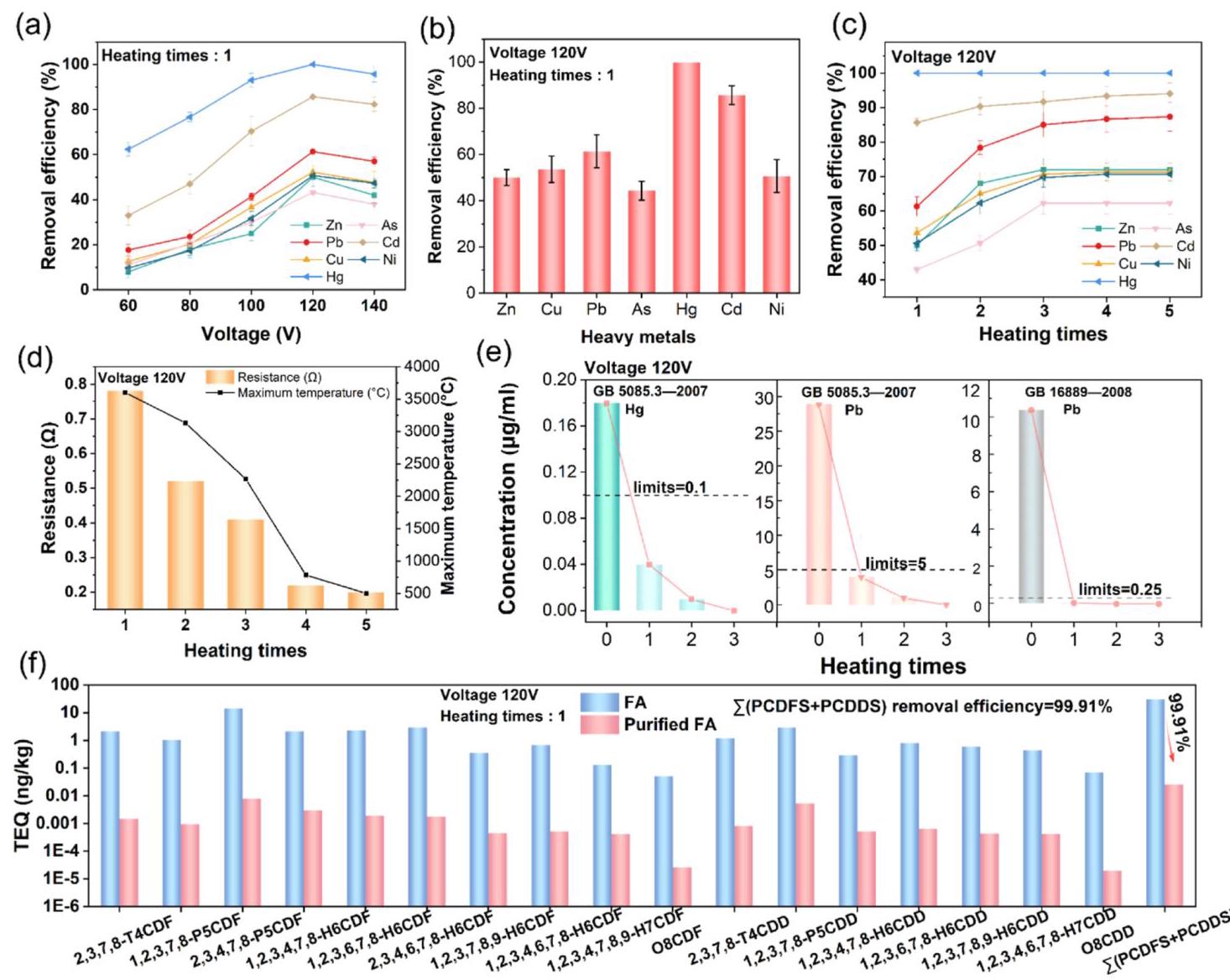
图4: (a) 五种初始电压下重金属去除效率; (b) 120V初始电压下重金属去除效率; (c) 1-5次加热下重金属去除效率; (d) 多次加热下电阻和最高温度变化; (e) 多次加热后飞灰中Hg和Pb的浸出浓度; (f) 超快碳热过程前后飞灰中二噁英的TEQ浓度
分析结果: 120V初始电压下重金属去除效果最佳,经过三次加热循环后去除效率显著提高。飞灰中Hg和Pb的浸出浓度在一次加热后即低于中国标准限值。二噁英去除率达到99.91%,证明超快碳热过程能有效降解这些持久性有机污染物。
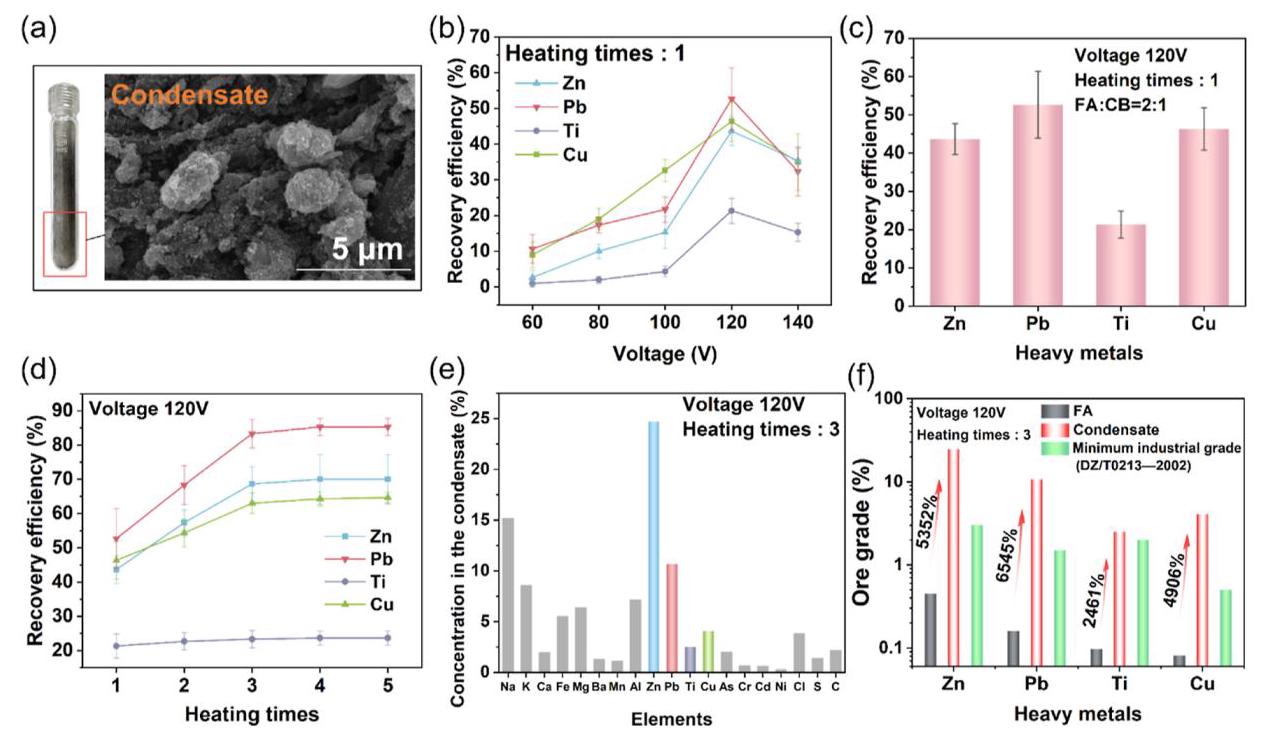
图5: (a) 回收管中收集的冷凝物; (b) 五种初始电压下重金属回收效率; (c) 120V初始电压下重金属回收效率; (d) 1-5次加热下重金属回收效率; (e) 120V初始电压下三次加热收集的冷凝物中元素浓度; (f) 飞灰、冷凝物中Zn、Pb、Ti和Cu的品位与最低工业要求的比较
分析结果: 冷凝物主要由微米和纳米颗粒组成,富含Zn、Pb、Ti和Cu等有价值元素。经过三次加热后,冷凝物中这些元素的浓度显著高于飞灰中的原始浓度,且远高于矿石的最低工业品位,具有很高的回收价值。
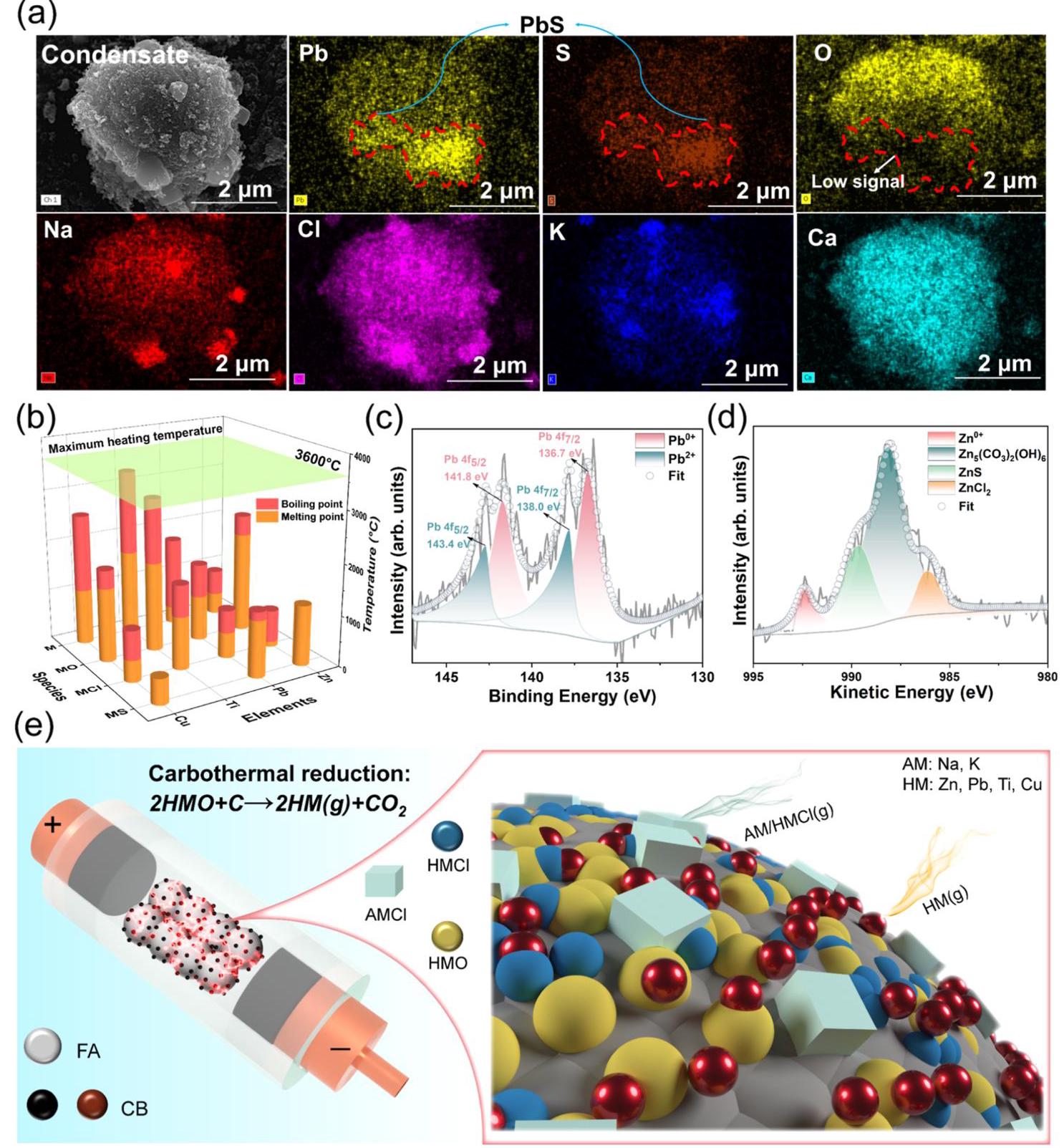
图6: (a) 收集固体的SEM图像和Pb、S、O、Na、K、Ca、Cl的EDS图谱; (b) Zn、Pb、Ti和Cu的元素、氧化物、氯化物和硫化物状态的熔点和沸点; (c) 120V初始电压生成冷凝物的Pb XPS精细谱; (d) 120V初始电压生成冷凝物的Zn LMM Auger谱; (e) 超快碳热过程中重金属挥发机制示意图
分析结果: EDS和XPS分析表明冷凝物中Pb主要以PbS和元素Pb形式存在,Zn则以ZnS、元素Zn、ZnCl₂和Zn₅(CO₃)₂(OH)₆形式存在。高温条件下发生了还原和硫化反应,促进了重金属的挥发和转化。不同重金属化合物的熔点和沸点差异解释了其挥发行为的差异。
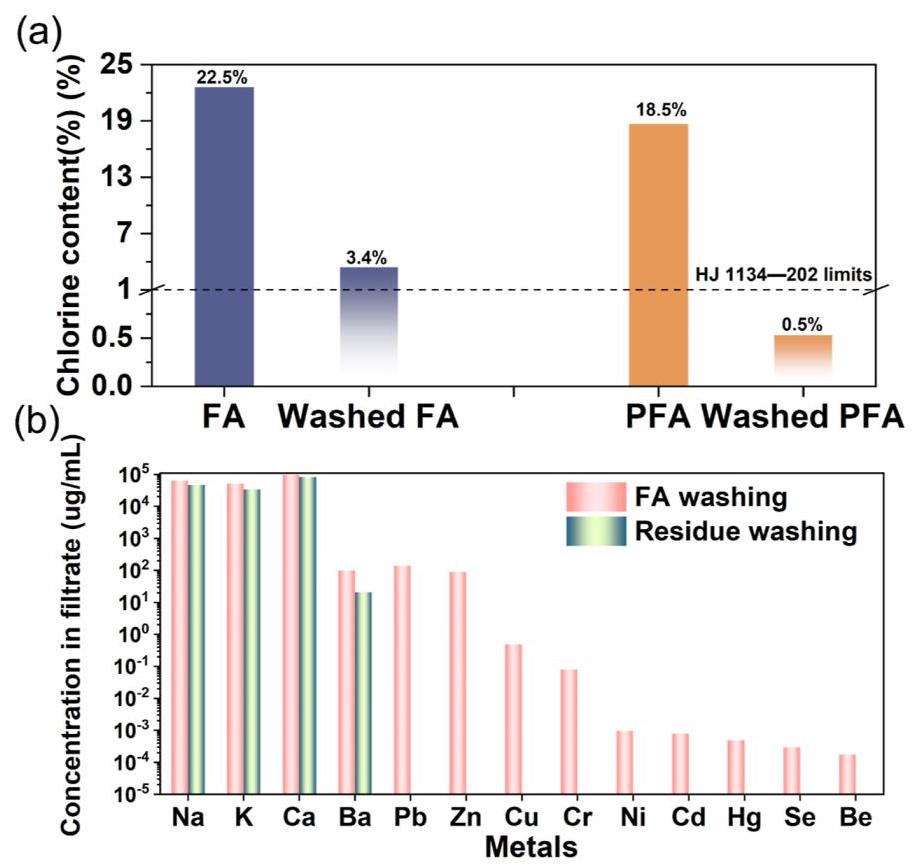
图7: (a) 飞灰和净化飞灰(PFA)的氯含量; (b) 飞灰洗涤和PFA洗涤滤液中的金属浓度
分析结果: 超快碳热过程将飞灰中的氯含量从22.5%降至18.5%,再经过水洗后可进一步降至0.5%,显著优于直接水洗的效果(仅降至3.4%)。PFA洗涤滤液中重金属浓度极低,几乎不含重金属污染,有利于后续氯化钠和氯化钾的提取和纯化。
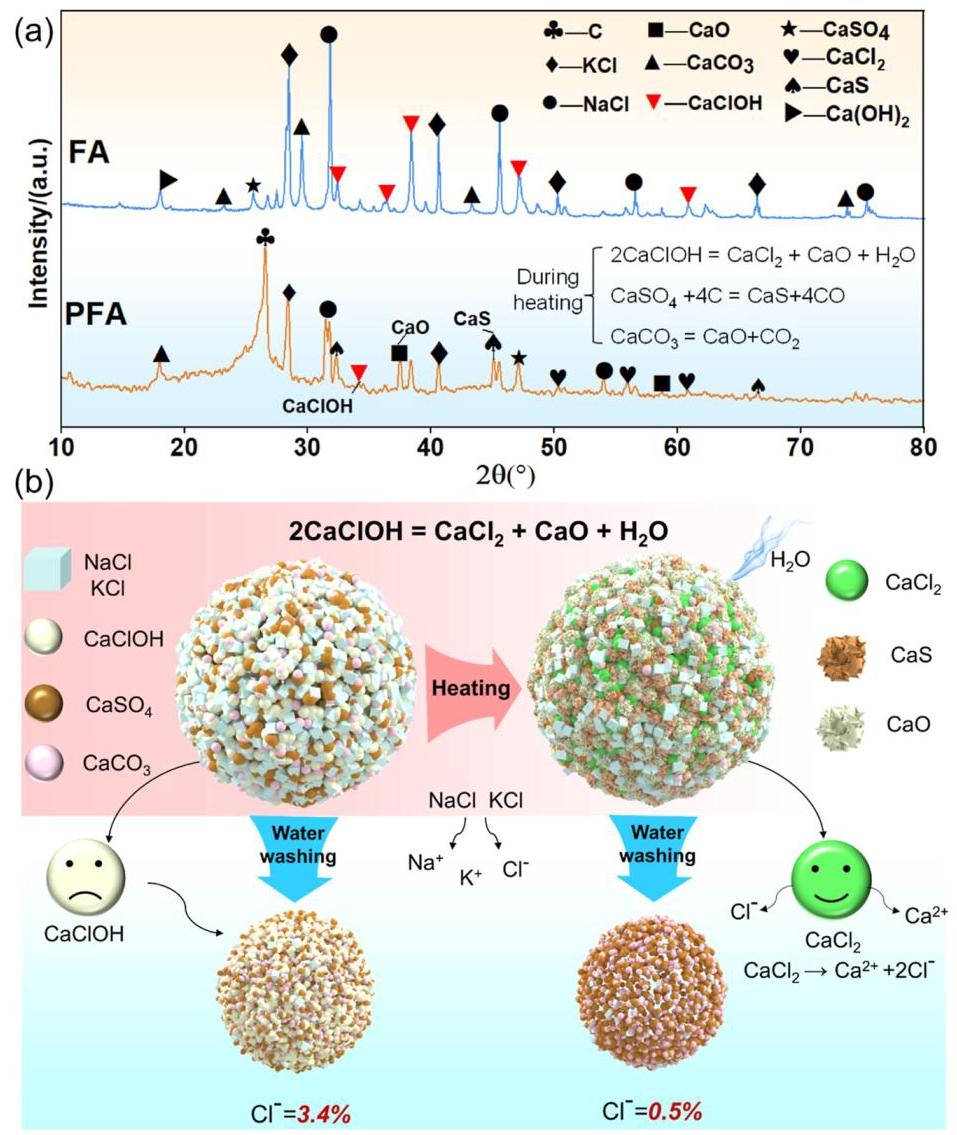
图8: (a) 飞灰和净化飞灰(PFA)的XRD图谱; (b) 超快碳热过程增强飞灰洗涤过程中氯溶解机制的示意图
分析结果: XRD分析显示超快碳热过程后CaClOH峰显著减少,同时出现CaO和CaCl₂峰,证明高温下CaClOH分解为水溶性CaCl₂和CaO。这一机制解释了为什么超快碳热处理后的飞灰在水洗过程中氯去除效果更好,因为难溶的CaClOH转化为了易溶的CaCl₂。