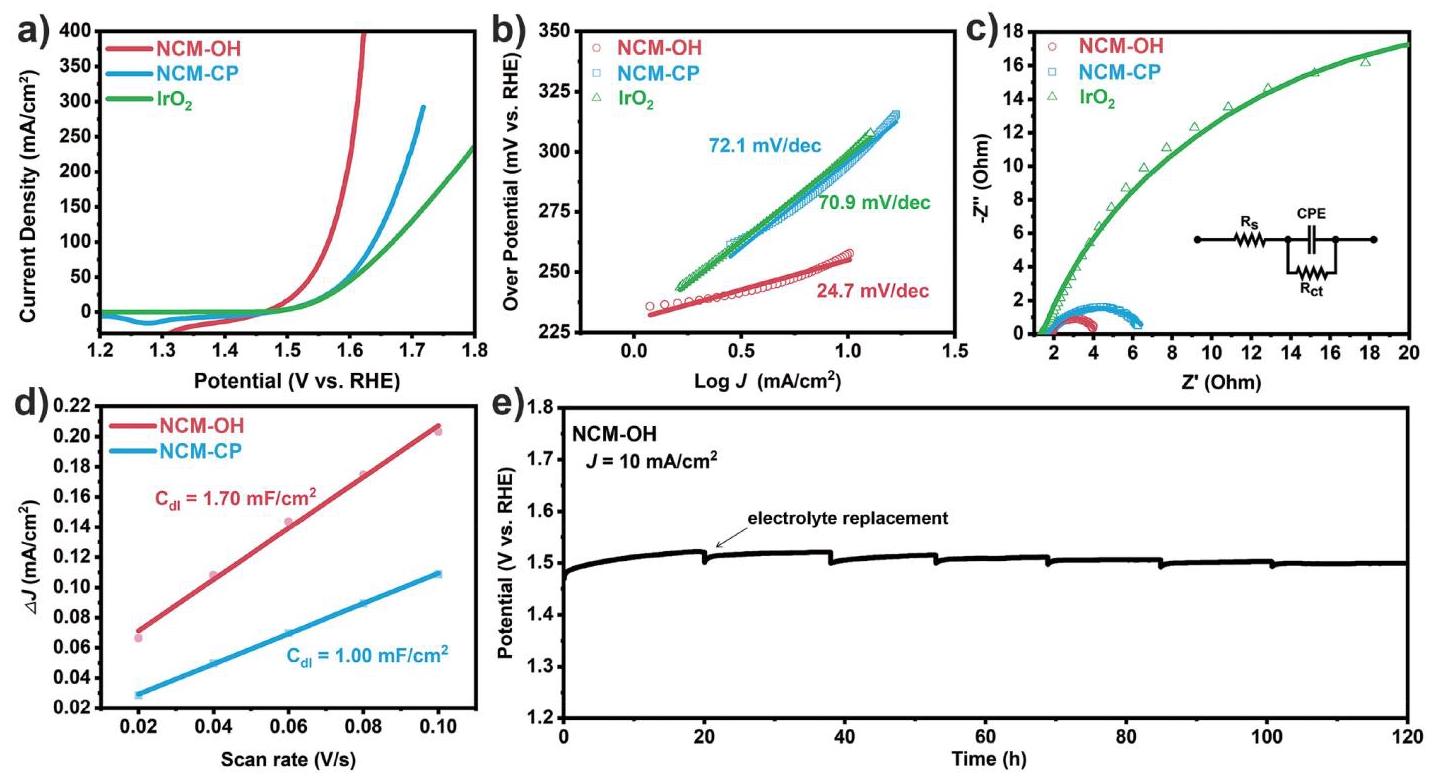
该图展示了NCM-OH催化剂在1.0 M KOH中使用标准三电极电池进行的OER活性测试。从图3a的极化曲线可以清楚地观察到,NCM-OH催化剂在10 mA/cm²下的过电位为257 mV,明显低于对照样品NCM-CP(295 mV)和IrO₂(298 mV)。
从相应极化曲线得到的Tafel斜率显示了不同催化剂的电催化动力学(图3b)。NCM-OH的Tafel斜率(24.7 mV/dec)远小于其他两个样品NCM-CP(72.1 mV/dec)和IrO₂(70.9 mV/dec),表明NCM-OH具有最佳的电化学动力学。结果表明,具有多金属氢氧化膜的NCM-OH对OER表现出优异的催化活性。
NCM-OH的电荷转移能力和稳定性也是评估催化剂性能的重要指标。图3c显示了电化学阻抗谱(EIS),提供了催化剂的必要电荷转移信息。NCM-OH的电荷转移电阻(Rct)为2.26Ω,而NCM-CP和IrO₂的Rct值分别为5.14Ω和47.84Ω。较低的Rct表明NCM-OH具有更有效的电荷转移和更快的界面反应动力学。
此外,与对照样品NCM-CP(Cdl = 1.00 mF/cm²)相比,NCM-OH表现出更高的双电层电容(Cdl)为1.70 mF/cm²(图3d),这与NCM-OH更大的电化学活性表面积(ECSA)直接相关。结果证实,NCM-OH的薄膜结构对于增强其电催化活性至关重要。
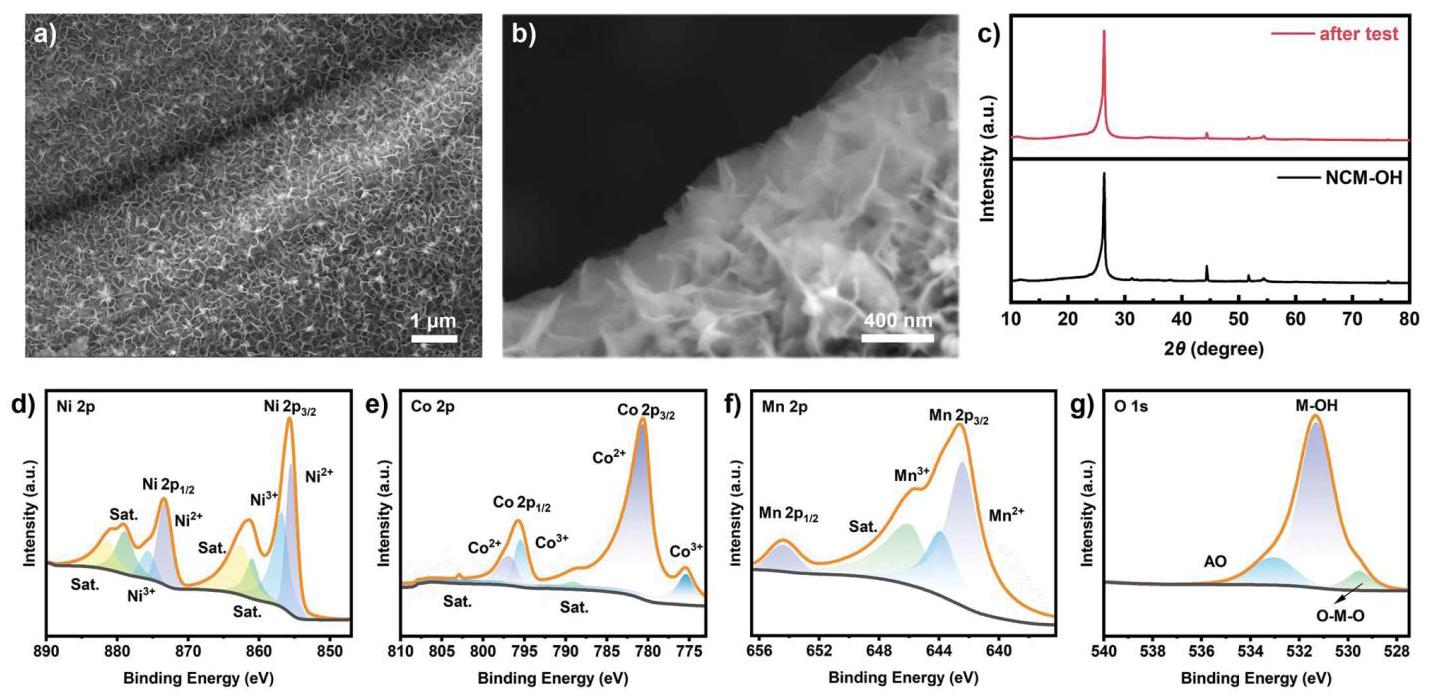
此外,图3e显示了计时电位测量,以评估NCM-OH的稳定性。在10 mA/cm²恒定电流下测试120小时后,NCM-OH的过电位仅增加了12 mV,表明其优异的电化学稳定性。与先前报道的过渡金属基催化剂相比,NCM-OH表现出更低的过电位和Tafel斜率,进一步证实了其优异的OER催化性能。