Modulating Spin State of Ni Single Atomic Center for High-Performance Electrocatalytic Carbon Dioxide Reduction
调控镍单原子中心自旋态实现高性能电催化二氧化碳还原
Zhen Chen†, Jiankang Liu†, Jianpeng Li†
通讯作者: Zhiyuan Wang (wangzhiy@zzu.edu.cn), Zhongyi Liu (liuzhongyi@zzu.edu.cn)
郑州大学 (Zhengzhou University)
DOI: 10.1002/anie.202506845
PDF原文
Angewandte Chemie International Edition, 2025
论文亮点
- 通过快速焦耳加热策略成功合成了具有不同氮配位类型(吡啶氮和吡咯氮)的镍单原子催化剂,并保持了前驱体的氮构型。
- 磁化率测量表明,吡啶氮配位诱导镍中心形成高自旋态,而吡咯氮配位则稳定低自旋态。高自旋态Ni-Npyridinic-C催化剂在电催化CO2还原中表现出卓越的活性和选择性。
研究背景
- 电催化二氧化碳还原(CO2RR)是将CO2转化为有价值化学品和合成燃料的有效途径,有助于缓解大气中CO2浓度并同时提供有价值的原料。
- 单原子催化剂(SACs)因其接近100%的金属原子利用率和独特的电子结构,在CO2RR中展现出巨大潜力。然而,关于配位氮物种对活性中心自旋态和催化性能影响的研究仍然缺乏。
- 金属活性中心的自旋态由其3d轨道电子的占据模式决定,通过改变中间体的吸附强度、反应路径的选择性和电子转移效率来显著影响催化性能。
研究方法
本研究采用气体保护的快速焦耳加热策略合成两种不同的镍单原子催化剂(Ni-Npyridinic-C 和 Ni-Npyrrolic-C)。具体步骤如下:
- 合成过程: 温度在5秒内快速升至2000°C,使镍金属配合物前驱体在高温下短时间内快速碳化。此快速碳化过程中,镍配合物的构型和配位氮类型来不及改变,导致Ni和N快速掺杂到XC-72碳载体中。
- 结构表征: 使用高分辨率透射电子显微镜(HRTEM)、像差校正高角环形暗场扫描透射电子显微镜(HAADF-STEM)和元素映射确认了镍的单原子分散状态。通过X射线吸收精细结构谱(XAFS)、X射线吸收近边结构谱(XANES)和X射线光电子能谱(XPS)技术确定了催化剂的配位结构(Ni-N4)和氮物种类型(吡啶氮或吡咯氮)。
- 自旋态测定: 通过磁化率(M-T)测量确定了Ni-Npyridinic-C中的Ni中心处于高自旋态,而Ni-Npyrrolic-C中的Ni中心处于低自旋态。
- 电化学性能测试: 在标准三电极H型电解池和气体扩散流通池中评估了催化剂的CO2RR性能,包括线性扫描伏安法(LSV)、法拉第效率(FE)、部分电流密度、转换频率(TOF)和稳定性测试。
- 机理研究: 采用原位衰减全反射红外光谱(ATR-IR)、电子顺磁共振(EPR)、投影态密度(PDOS)分析、晶体轨道汉密尔顿布居(COHP)分析和密度泛函理论(DFT)计算等手段深入探究了自旋态对催化活性和反应机理的影响。
- 锌-CO2电池应用: 构建了以Ni-Npyridinic-C为阴极的锌-CO2电池,评估其放电性能、功率密度和循环稳定性。
主要结论
- 成功通过配位氮调控实现了镍单原子中心自旋态(高自旋 vs. 低自旋)的调制,高自旋态Ni-Npyridinic-C催化剂表现出优异的CO2电还原活性和CO选择性。
- Ni-Npyridinic-C在H型电解池中于-0.7 V (vs. RHE) 下实现了98.8%的CO法拉第效率,并在-0.4 V 至 -1.2 V宽电位范围内保持90%以上。在流通池中,在碱性、中性和酸性电解液中均能实现>99%的CO法拉第效率和超过450 mA cm-2的工业级CO部分电流密度。
- 理论计算表明,高自旋态增强了Ni的d轨道分散,加强了与CO2分子π*轨道的杂化,稳定了*COOH中间体,从而降低了*COOH形成的能垒,加速了CO2活化动力学。
图1: 催化剂的合成与形貌表征
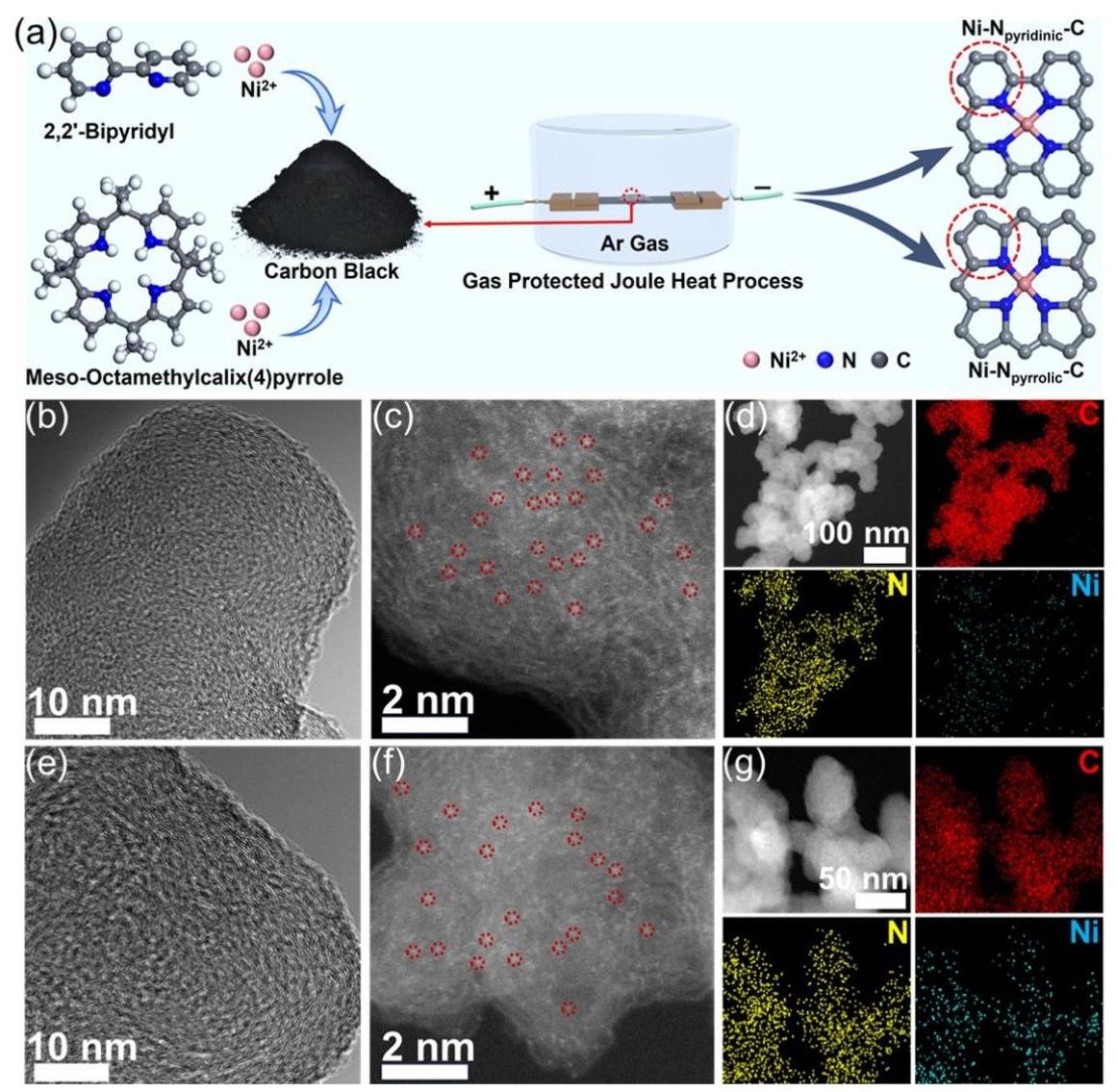
图1. (a) Ni-Npyrrolic-C 和 Ni-Npyridinic-C 的合成示意图。(b) TEM图像, (c) HAADF-STEM图像 和 (d) Ni-Npyridinic-C 的元素分布映射图像。(e) TEM图像, (f) HAADF-STEM图像 和 (g) Ni-Npyrrolic-C 的元素分布映射图像。
分析结果: 图1a展示了通过快速焦耳加热法合成两种催化剂的策略。图1b, e的TEM图像显示了继承自XC-72碳黑的不规则类石墨碳结构。图1c, f的HAADF-STEM图像中未观察到金属纳米颗粒,均匀分布的亮点证实了镍的单原子分散状态。图1d, g的元素映射进一步证实了Ni和N元素在整个碳载体上的均匀分布。这些结果表明成功合成了原子级分散的镍单原子催化剂。
图2: 催化剂的精细结构表征
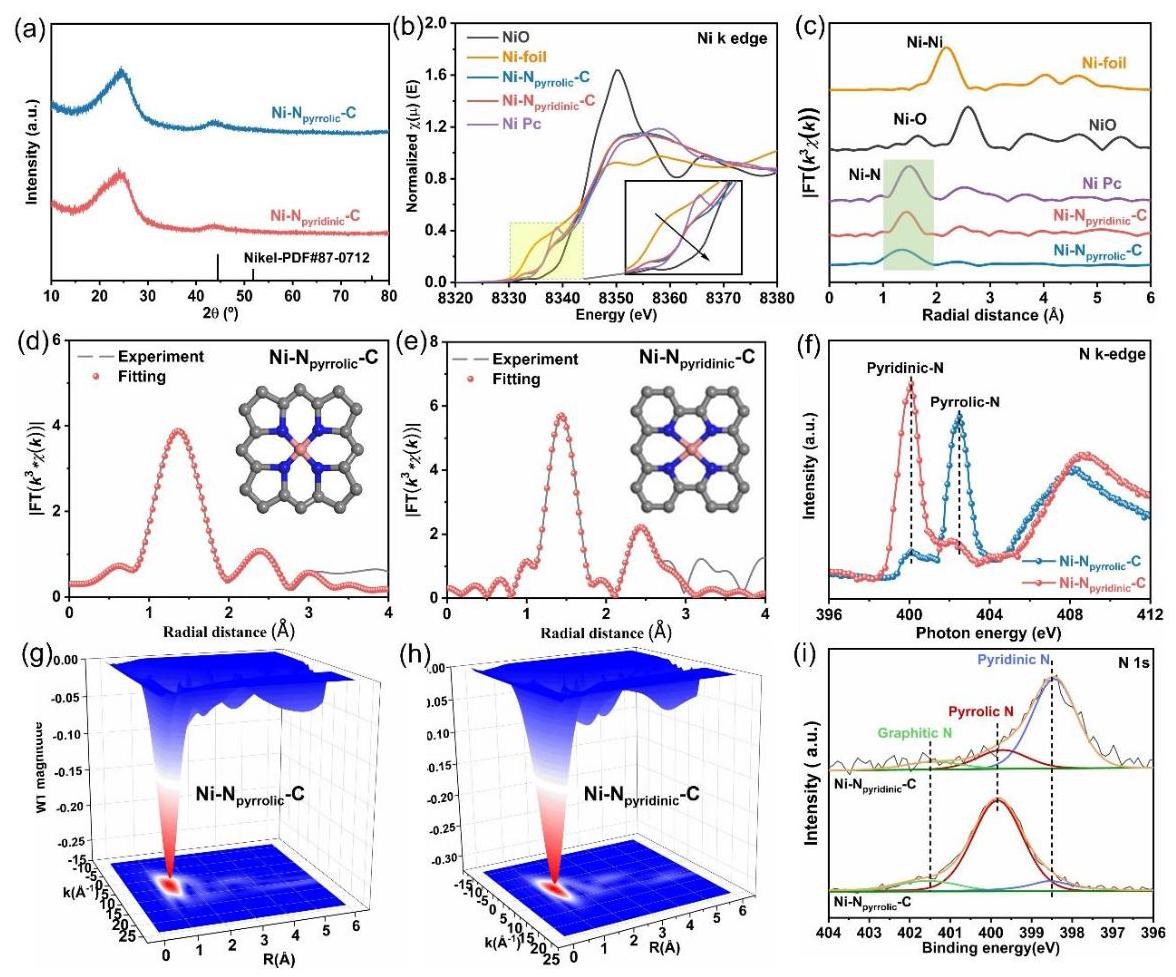
图2. (a) Ni-Npyridinic-C 和 Ni-Npyrrolic-C 的XRD谱图。(b) 归一化的Ni K边XANES谱和 (c) Ni K边的傅里叶变换k3加权EXAFS谱(Ni-Npyrrolic-C, Ni-Npyridinic-C 及参比样)。(d-e) R空间中Ni-Npyrrolic-C 和 Ni-Npyridinic-C 的Ni K边FT-EXAFS拟合结果。(f) Ni-Npyrrolic-C 和 Ni-Npyridinic-C 的N K边XAFS谱。(g-h) Ni-Npyrrolic-C 和 Ni-Npyridinic-C 的k2加权Ni K边EXAFS谱的小波变换。(i) Ni-Npyrrolic-C 和 Ni-Npyridinic-C 的N 1s XPS谱。
分析结果: XRD谱图(图2a)显示两种催化剂只有碳的宽峰,无金属Ni衍射峰,证实无晶态Ni物种。XANES谱(图2b)表明白线峰位于NiO和Ni箔之间,接近NiPc,表明Ni的氧化态介于0到+2之间。EXAFS谱(图2c)在~1.4 Å处的主峰归属于Ni-N配位,无Ni-Ni峰,证实Ni的单原子分散。定量EXAFS拟合(图2d,e)证实两种催化剂中Ni均与四个N原子配位。N K边XANES(图2f)和N 1s XPS(图2i)明确区分了两种催化剂的主要氮类型:Ni-Npyridinic-C中以吡啶氮为主(83.4 at.%),Ni-Npyrrolic-C中以吡咯氮为主(85.6 at.%)。这些分析确证了两种催化剂具有相同的Ni-N4配位结构但主要配位氮类型不同。
图3: 电催化CO2还原性能
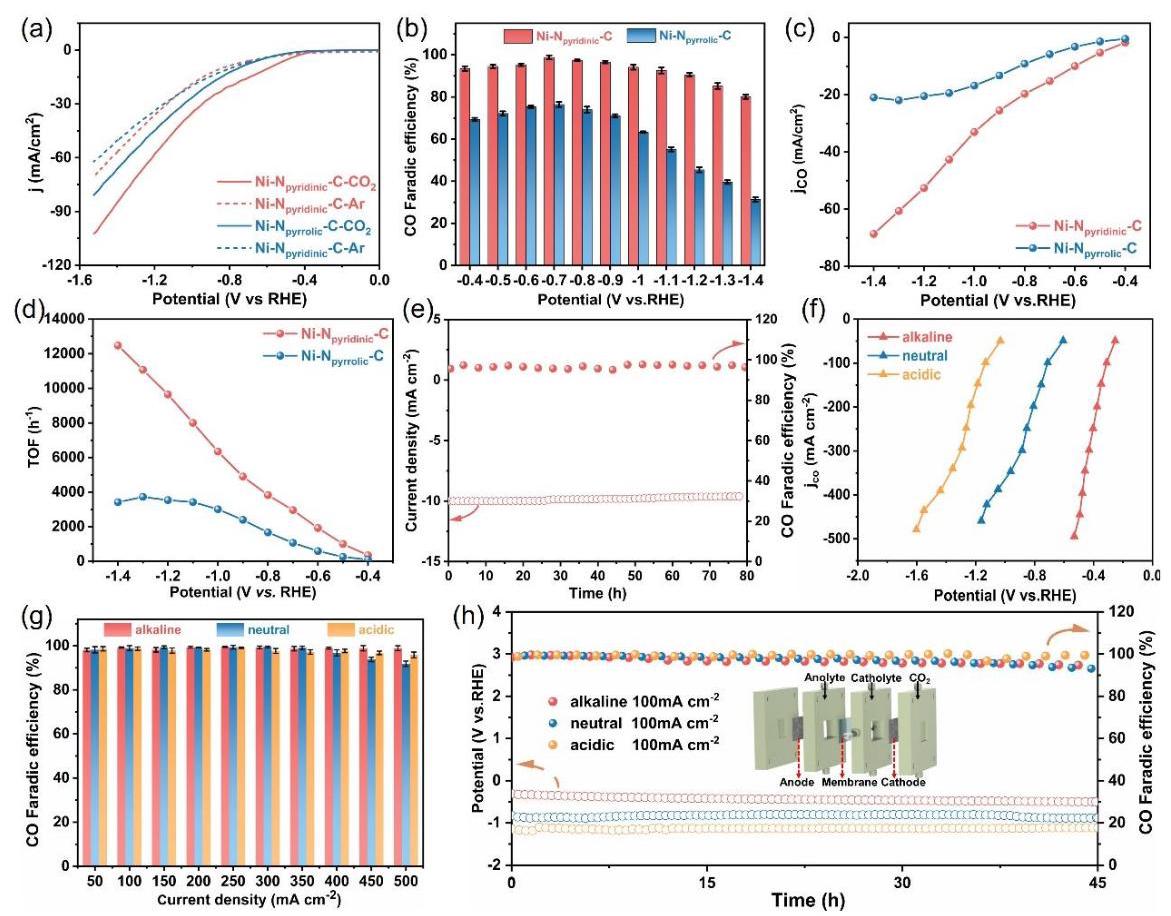
图3. (a) Ni-Npyrrolic-C 和 Ni-Npyridinic-C 在CO2/Ar饱和电解液中的LSV曲线。(b) H型电解池中Ni-Npyrrolic-C 和 Ni-Npyridinic-C 的CO法拉第效率和 (c) CO部分电流密度。(d) Ni-Npyrrolic-C 和 Ni-Npyridinic-C 的TOF值。(e) Ni-Npyridinic-C 在H型电解池(0.5 M KHCO3电解液)中运行80小时的稳定性测试。(f) 流通池中Ni-Npyridinic-C在碱性、中性、酸性电解液中的CO部分电流密度和 (g) CO法拉第效率。(h) Ni-Npyridinic-C在流通池中的稳定性测试及气体扩散流通池示意图。
分析结果: Ni-Npyridinic-C在所有测试电位下均显示出比Ni-Npyrrolic-C更大的电流密度(图3a)和更高的CO法拉第效率(图3b),在-0.7 V时达到98.8%的最大FECO,且在-0.4 V至-1.2 V范围内保持90%以上。Ni-Npyridinic-C的CO部分电流密度(图3c)和TOF值(图3d)也显著更高。Ni-Npyridinic-C在H型电解池中表现出优异的稳定性,80小时内电流密度和FECO几乎无衰减(图3e)。在流通池中(图3f,g),Ni-Npyridinic-C在碱性、中性、酸性电解液中均能实现高FECO(>99%)和工业级CO部分电流密度(>450 mA cm-2)。在不同pH的电解液中进行的长时间稳定性测试(图3h, S24)也证明了其出色的耐久性。这些结果凸显了Ni-Npyridinic-C催化剂在实际应用中的巨大潜力。
图4: 锌-CO2电池性能
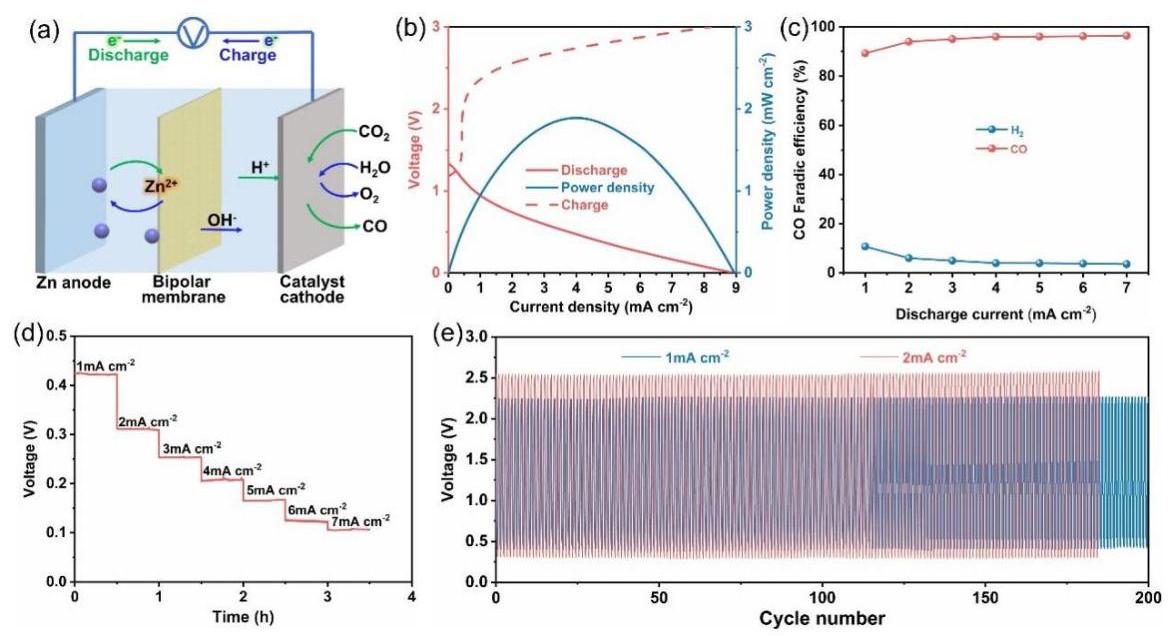
图4. (a) 水系锌-CO2电池结构示意图。(b) 以Ni-Npyridinic-C为电催化剂的锌-CO2电池的极化曲线和功率密度。(c) 放电过程中的CO和H2法拉第效率。(d) 不同电流密度下的放电曲线。(e) 不同电流密度下的充放电曲线。
分析结果: 基于Ni-Npyridinic-C催化剂构建了锌-CO2电池(图4a)。电池显示出明显的可充电行为(图4b)。在放电过程中,电池在4.0 mA cm-2的放电电流密度下可提供1.89 mW cm-2的最大功率密度(图4b)。放电产物检测表明(图4c),Ni-Npyridinic-C在放电过程中表现出优异的CO选择性,在7.0 mA cm-2时最大CO法拉第效率为96.0%,并在2.0-7.0 mA cm-2的宽电流密度范围内保持92.1%以上。在不同放电电流密度下,放电电压保持稳定(图4d)。在1 mA cm-2和2 mA cm-2电流密度下进行的恒流充放电循环测试(图4e)显示了电池的高稳定性,200次和180次循环后均未观察到明显的电压衰减。这表明组装的锌-CO2电池具有出色的稳定性,进一步证明了Ni-Npyridinic-C催化剂的适用性。
图5: 催化机理研究
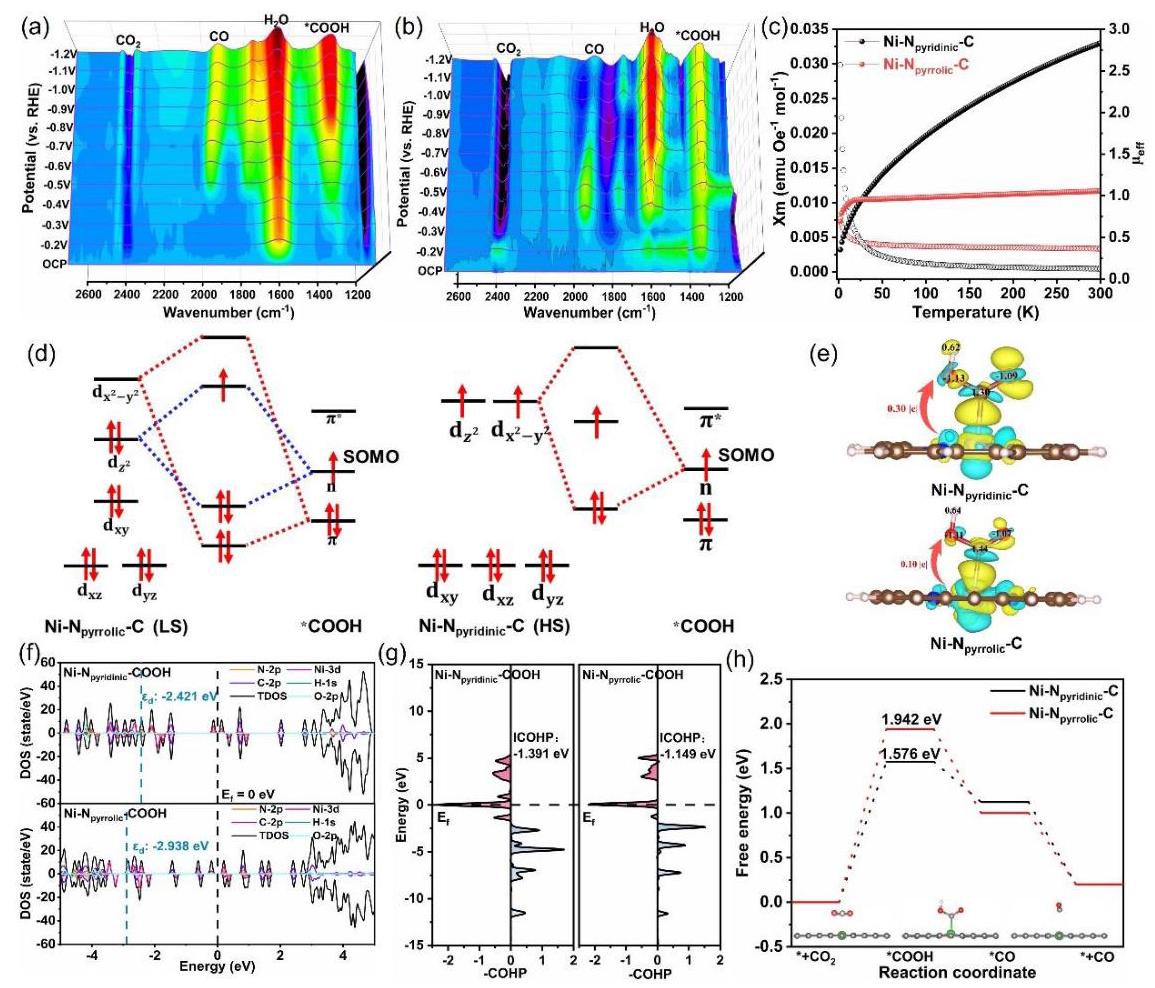
图5. (a) Ni-Npyridinic-C 和 (b) Ni-Npyrrolic-C 催化剂上CO2还原的原位ATR-FTIR光谱。(c) Ni-Npyridinic-C 和 Ni-Npyrrolic-C 的磁化率。(d) *COOH与Ni在Ni-Npyrrolic-C (LS) 和 Ni-Npyridinic-C (HS) 上的轨道相互作用。(e) *COOH吸附在Ni-Npyridinic-C 和 Ni-Npyrrolic-C 上的电荷密度差和Bader电荷分析。(f) Ni-Npyridinic-C 和 Ni-Npyrrolic-C 上Ni和*COOH的投影态密度(PDOS)。(g) Ni-Npyridinic-C 和 Ni-Npyrrolic-C 上Ni-*COOH的晶体轨道汉密尔顿布居(COHP)分析。(h) CO2RR在Ni-Npyridinic-C 和 Ni-Npyrrolic-C 上的自由能图。
分析结果: 原位ATR-IR光谱(图5a,b)检测到了*COOH、H2O、CO和CO2的信号,且Ni-Npyridinic-C上的*COOH和CO峰强度显著更大,表明其更高的催化活性。磁化率测量(图5c)确定Ni-Npyridinic-C和Ni-Npyrrolic-C中Ni中心分别处于高自旋态(μeff = 2.83 μB, 2个未配对电子)和低自旋态(μeff = 1.05 μB, 0个未配对电子)。PDOS分析(图5f, S30)显示高自旋态Ni的d轨道能级分布更分散。COHP分析(图5g)表明Ni-Npyridinic-C与*COOH的相互作用更强(ICOHP = -1.391 eV vs. -1.149 eV)。Bader电荷分析(图5e)显示Ni-Npyridinic-C向*COOH转移了更多电荷(0.30e vs. 0.10e)。自由能图(图5h)表明*COOH的形成是决速步,且Ni-Npyridinic-C上*COOH形成的能垒(1.57 eV)显著低于Ni-Npyrrolic-C(1.94 eV)。这些结果综合表明,高自旋态通过增强Ni与*COOH中间体的相互作用、促进电子转移,从而降低了反应能垒,提高了CO2RR活性和选择性。
研究总结图示
通过气体保护的快速焦耳加热策略开发了两种具有不同配位氮物种的Ni-N4C单原子电催化剂。吡啶型氮配位的Ni-Npyridinic-C在H型电解池中表现出优于吡咯型氮配位的Ni-Npyrrolic-C的电催化CO2还原活性,CO法拉第效率接近100%。值得注意的是,在碱性、中性和酸性电解液中均实现了优异的催化活性和工业级CO部分电流密度。出色的耐久性和CO选择性源于通过不同配位氮物种调控Ni中心的自旋态,这显著加强了Ni中心与*COOH中间体的相互作用并促进了电子转移,导致*COOH形成的能垒降低和*COOH进一步还原的反应动力学加快。





