黑粉中酸可提取电池金属的分析
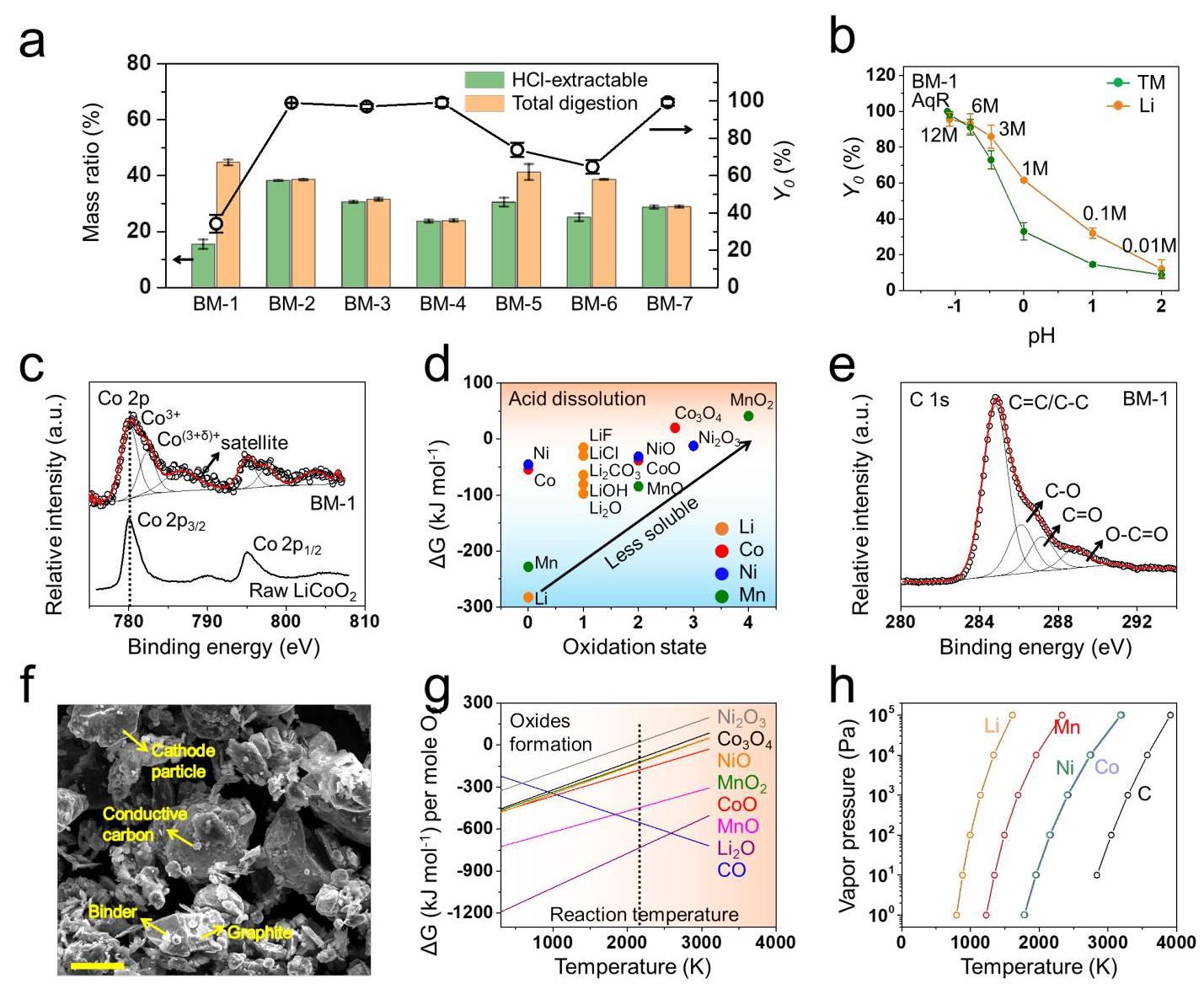
图1: 黑粉中酸可提取电池金属。(a)不同黑粉类型中HCl可提取电池金属含量和总定量;(b)BM-1中锂和过渡金属的pH依赖性浸出性;(c)BM-1和原始LiCoO₂的高分辨率Co 2p光谱;(d)金属及其相应金属化合物在1M HCl中的溶解吉布斯自由能;(e)BM-1的高分辨率C 1s光谱;(f)BM-1的SEM图像;(g)一氧化碳和各种金属氧化物的埃林汉姆图;(h)各种电池金属和碳的蒸气压-温度关系
分析结果:研究表明,黑粉中的电池金属含量远高于自然资源中的含量,是电池金属供应的优选来源。酸浸出回收率较低的原因在于有限的热力学和缓慢的溶解动力学。XPS分析证实部分脱锂导致钴的氧化态增加,使得金属化合物在酸溶液中溶解的热力学条件变差。此外,SEI钝化层影响了酸浸出速率,导致溶解动力学缓慢和浸出性低。
FJH活化提高电池金属回收率
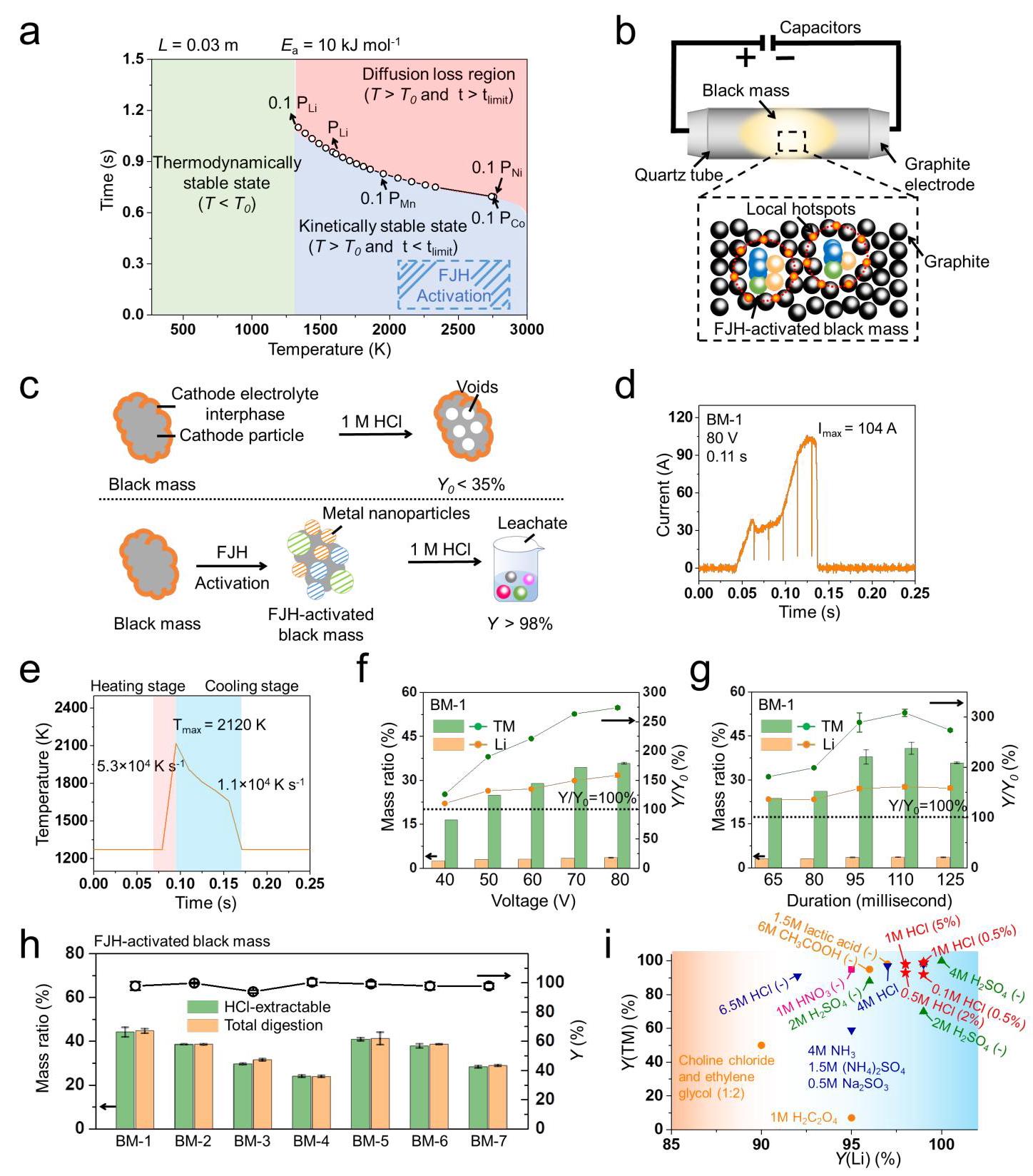
图2: FJH活化提高不同黑粉中电池金属回收率。(a)强调FJH活化过程的时间和温度依赖性图;(b)黑粉FJH活化示意图;(c)有无FJH活化的酸浸出结果;(d)FJH活化条件为80V和0.11秒时的电流-时间曲线;(e)FJH活化条件为80V和0.11秒时的实时温度测量;(f)FJH活化BM-1的HCl可提取电池金属含量、回收率增加与FJH电压的关系;(g)FJH活化BM-1的HCl可提取电池金属含量、回收率增加与FJH持续时间的关系;(h)各种FJH活化黑粉的HCl可提取电池金属含量和总定量,以及通过1M HCl从各种FJH活化黑粉中回收电池金属的回收率(Y);(i)不同浸出剂对锂和过渡金属回收率的比较
分析结果:随着闪蒸电压从40V增加到80V,锂和过渡金属的浸出性增加。在约80V和110ms时,1.0M HCl可提取的锂和过渡金属含量分别为35.2g/kg和407.0g/kg,对应锂和过渡金属的Y值约为98%。与黑粉的Y0相比,锂和过渡金属的回收率(Y/Y0)分别显著增加至约161%和309%。即使酸浓度降低100倍至0.01M HCl(pH2),FJH活化黑粉的锂和过渡金属Y值分别约为74%和70%,远高于相同浸出条件下黑粉的Y0值(锂约12%,过渡金属约9%)。
FJH活化提高电池金属提取能力的机制
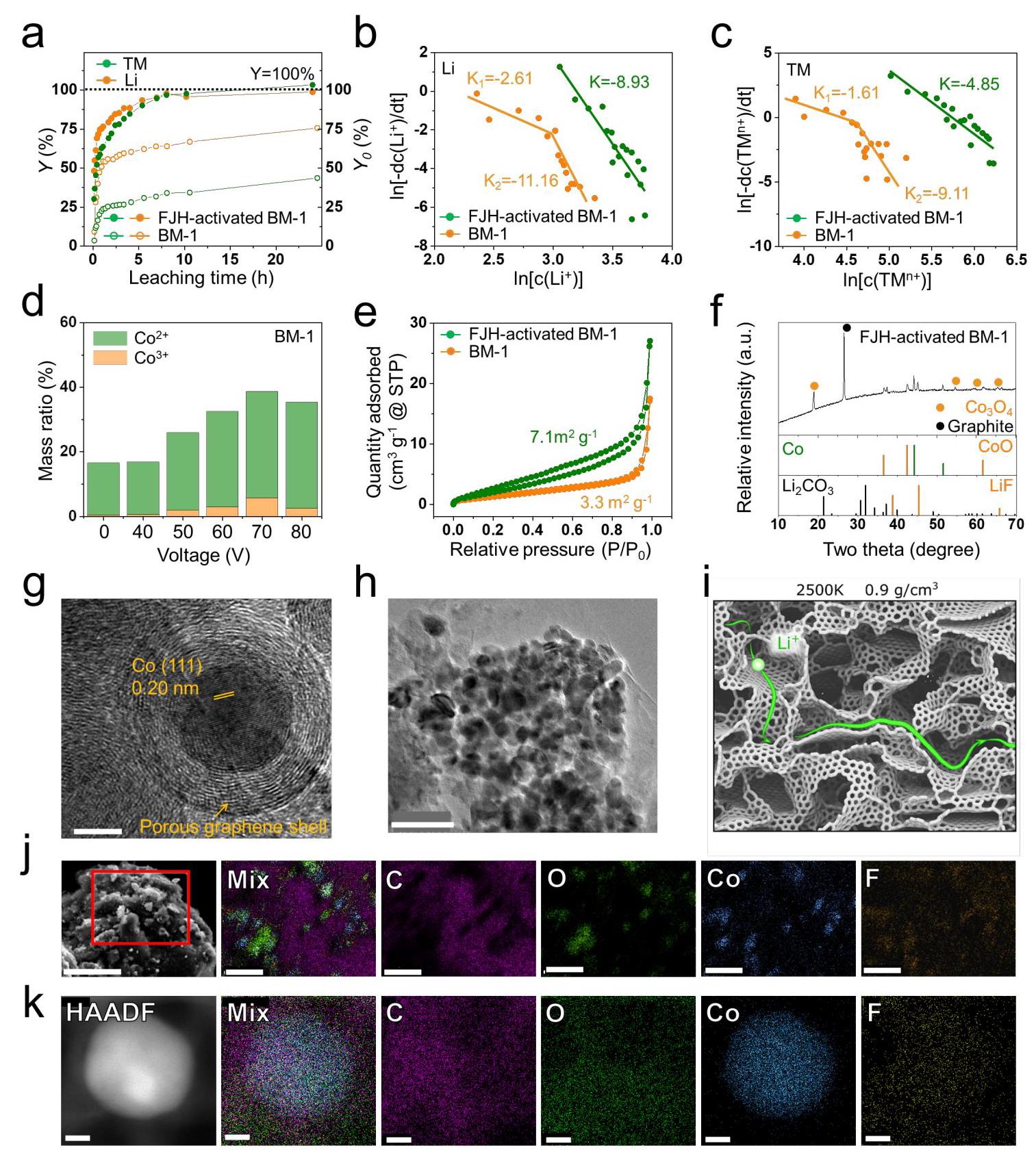
图3: FJH活化提高电池金属提取能力的机制。(a)BM-1(Y0)和FJH活化BM-1(Y)与1M HCl的动力学浸出回收率;(b)动力学锂浸出速率与浸出液中Li⁺浓度的关系;(c)动力学过渡金属浸出速率与浸出液中总过渡金属离子浓度的关系;(d)FJH活化BM-1的HCl可提取电池金属含量中Co²⁺、Co³⁺浓度与闪蒸电压的关系;(e)报告原始和FJH活化BM-1表面积的氮吸附和解吸曲线;(f)FJH活化BM-1的XRD图谱;(g)FJH活化BM-1的HR-TEM;(h)FJH活化BM-1的TEM图像;(i)Li⁺在2500K退火9ns末渗透部分石墨化非晶碳结构;(j)FJH活化BM-1二次颗粒的微观形态和相应元素分布;(k)FJH活化BM-1初级颗粒的纳米级形态和相应元素分布
分析结果:FJH活化黑粉的酸浸出动力学研究表明,其Y值增加速率快于黑粉的Yθ。即使经过约25小时,使用1.0M HCl时,锂和过渡金属的Y0仅分别约为76%和44%,而FJH活化黑粉几乎完全溶解了电池金属。平均而言,FJH活化黑粉的锂和过渡金属酸浸出速率分别比黑粉快约100倍和1000倍。UV-vis吸收光谱确定浸出液中钴离子的分布表明,过渡金属浸出效率的提高主要归因于浸出液中Co²⁺的增加,表明过渡金属的有效碳热还原。
FJH活化回收过程的经济和环境分析
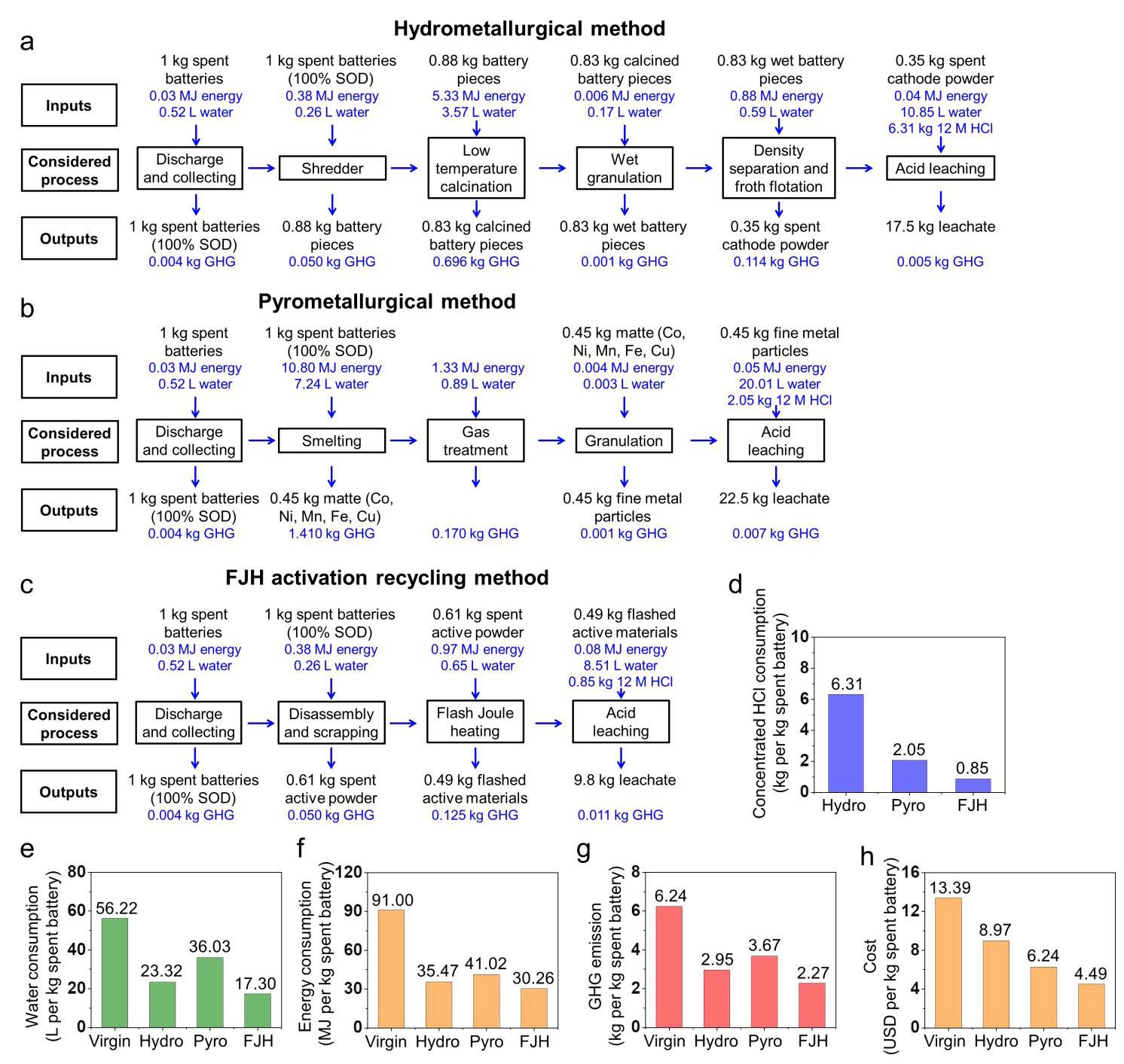
图4: FJH活化回收过程的经济和环境分析。(a-c)各种废锂离子电池回收路线的工艺流程图;(d)处理1kg废电池的浓缩12M HCl消耗量;(e-h)处理1kg废电池随后从浸出液生产约0.35kg阴极材料的水耗、能耗、温室气体排放和成本分析
分析结果:生命周期分析表明,与湿法冶金方法相比,FJH活化回收方法使浓缩HCl消耗减少约87%,水耗减少约26%,能耗减少约15%,温室气体排放减少约23%。与火法冶金方法相比,FJH活化回收方法使浓缩HCl使用减少约59%,水耗减少约52%,能耗减少约26%,温室气体排放减少约38%,反映了环境足迹的减少,导致估计成本降低约28%。处理1kg废电池生产约0.35kg阴极材料的估计成本比湿法冶金方法低约49%,比火法冶金方法低约28%。



