图1: 超高温焦耳加热制备rNC气凝胶示意图
分析结果
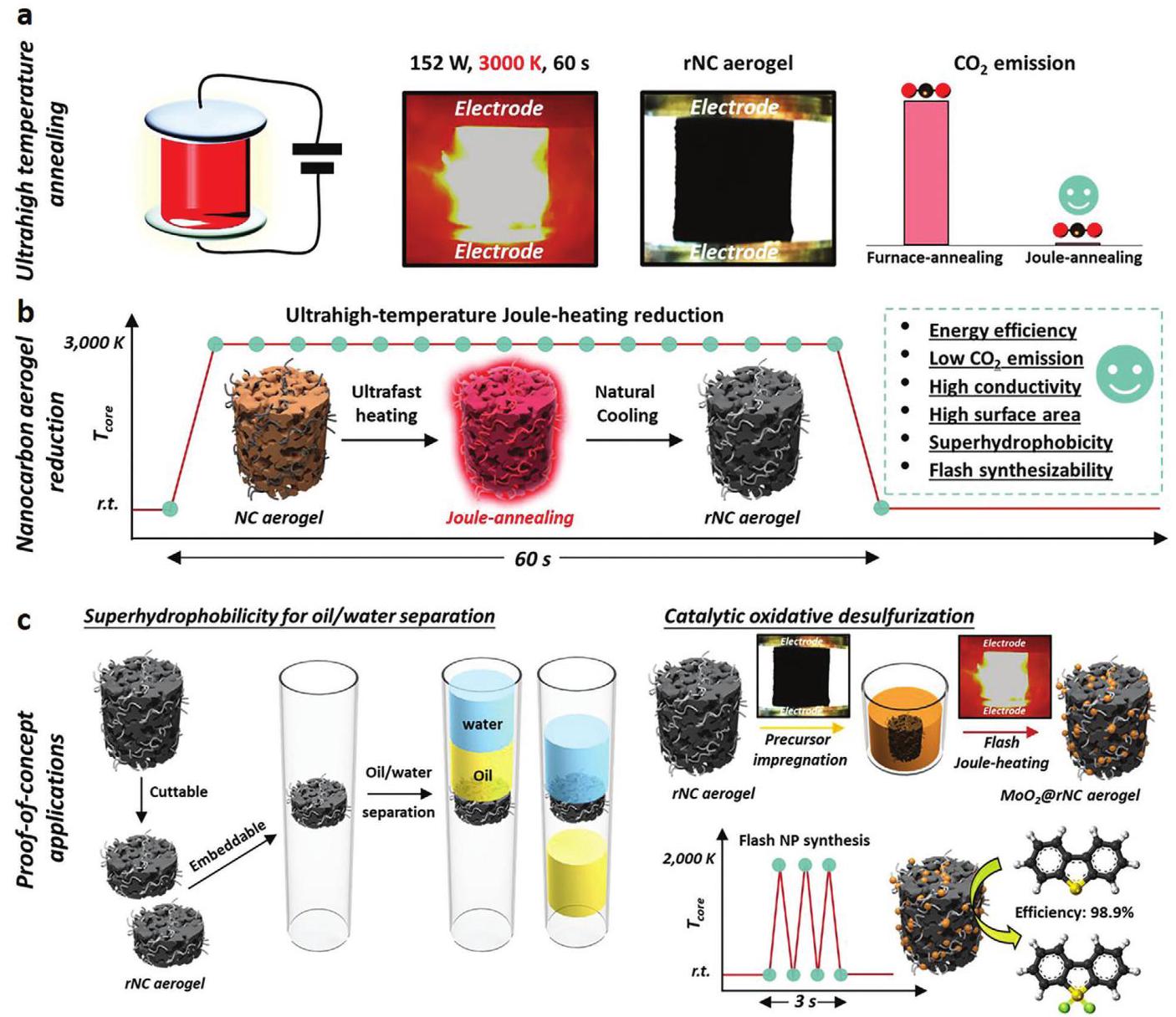
图1展示了通过超高温焦耳加热制备物理化学增强型rNC气凝胶的全过程。该方法的核心优势在于其极低的CO2排放和高效的能量利用。通过焦耳加热,纳米碳气凝胶在极短时间内(60秒)达到超高温(约3000K),实现了快速石墨化,显著改善了气凝胶的导电性、导热性和疏水性。制备的rNC气凝胶具有多功能应用潜力,包括油水分离和作为催化剂载体用于氧化脱硫反应。
第一作者: Dong Xia
通讯作者: Qun Li*, Yifei Xu*, Peng Huang*
本研究采用水热合成法制备了三维宏观纳米碳气凝胶,具体步骤如下:
焦耳加热测量在自制的焦耳加热装置中进行,在N2气氛下的密闭容器中进行。使用热电偶记录气凝胶表面和核心温度,通过1D热传导模型和幂律分析准确估算核心温度。

图1展示了通过超高温焦耳加热制备物理化学增强型rNC气凝胶的全过程。该方法的核心优势在于其极低的CO2排放和高效的能量利用。通过焦耳加热,纳米碳气凝胶在极短时间内(60秒)达到超高温(约3000K),实现了快速石墨化,显著改善了气凝胶的导电性、导热性和疏水性。制备的rNC气凝胶具有多功能应用潜力,包括油水分离和作为催化剂载体用于氧化脱硫反应。
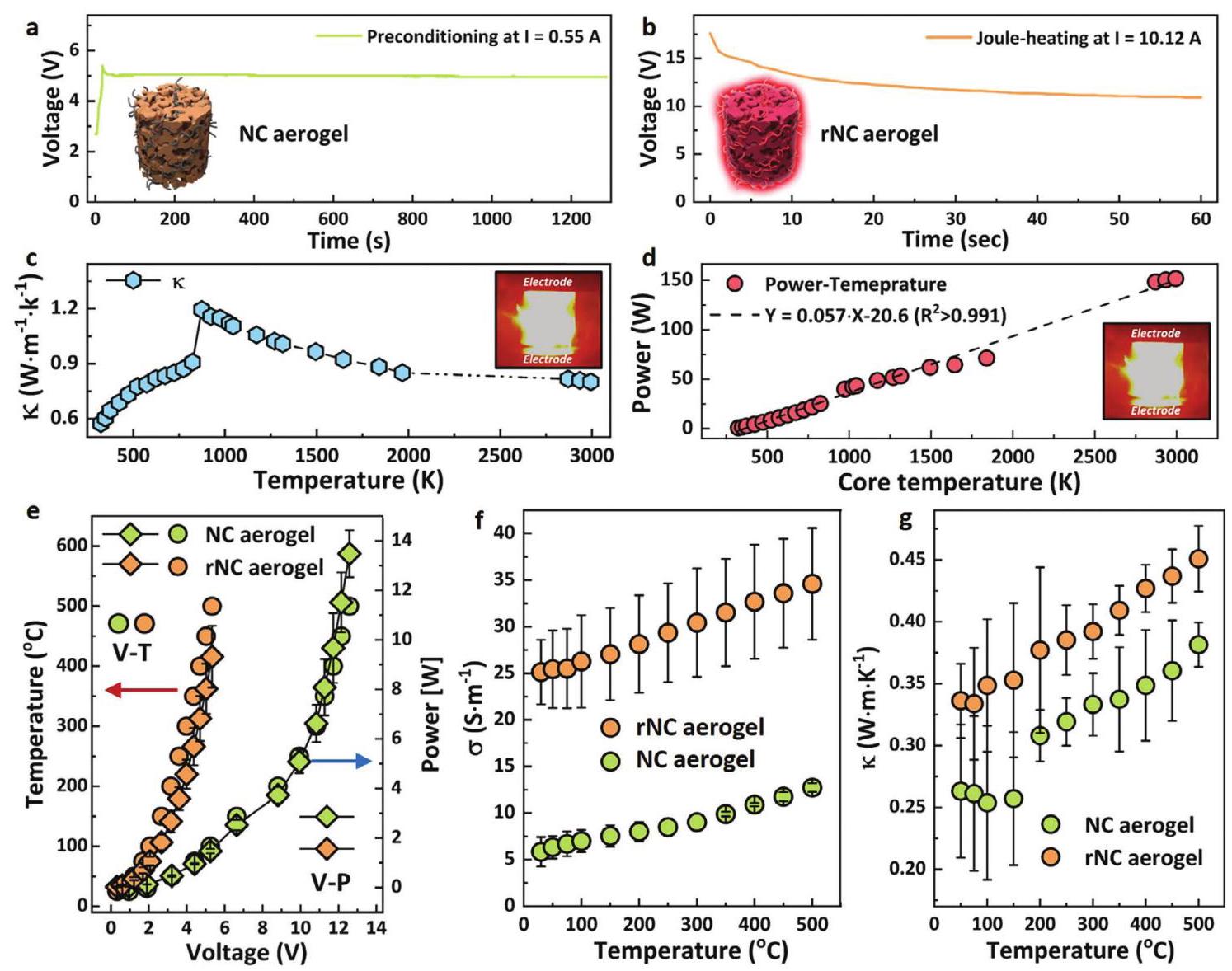
图2详细展示了焦耳加热过程及其对纳米碳气凝胶性能的影响。通过预处理去除水分和稳定气凝胶的焦耳加热能力后,在10.12A电流下进行60秒的闪速焦耳加热,使气凝胶达到超高温,产生强烈的黑体辐射现象。Umklapp散射分析表明,rNC气凝胶的温度可达到约3000K,远超过传统炉温(通常低于1573K)。功率-温度关系的高线性度(R²>0.991)验证了估算气凝胶核心温度方法的可靠性,并证明了焦耳加热实现精确温度控制的能力。rNC气凝胶表现出显著改善的电导率(25Sm⁻¹)和热导率(0.33Wm⁻¹K⁻¹),这归因于恢复的石墨纳米结构促进了电子和声子的移动。
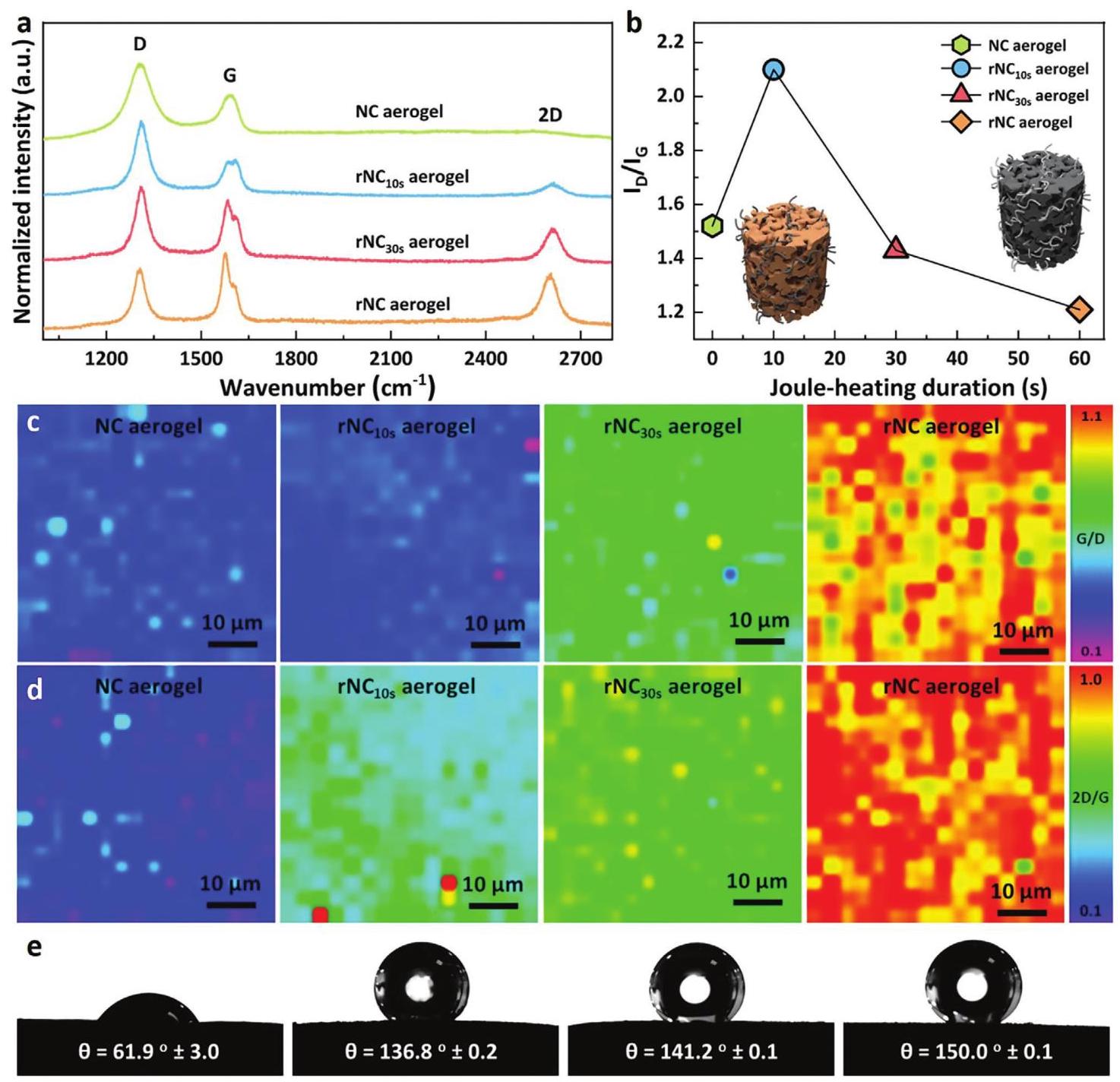
图3通过拉曼光谱和接触角测量分析了焦耳加热对纳米碳气凝胶石墨化程度和疏水性的影响。拉曼光谱显示三个明显的波段:约1313cm⁻¹的D带(缺陷带)、约1578cm⁻¹的G带(代表石墨烯平面构型的主要面内振动模式)和约2602cm⁻¹的2D带(不同面内振动的二阶泛音)。ID/IG比值广泛用于评估有缺陷纳米碳材料的石墨化程度,随着加热时间的变化呈现非线性趋势,符合Tuinstra-Koenig关系。经过60秒焦耳加热的rNC气凝胶经历了显著的结晶度恢复。拉曼映射显示了石墨再结晶的二维均匀性,证实了焦耳加热下热还原的均匀性。闪速焦耳加热过程的一个关键成果是rNC气凝胶实现了超疏水性,接触角达到150°,与仅61.9°的亲水性NC气凝胶形成鲜明对比。
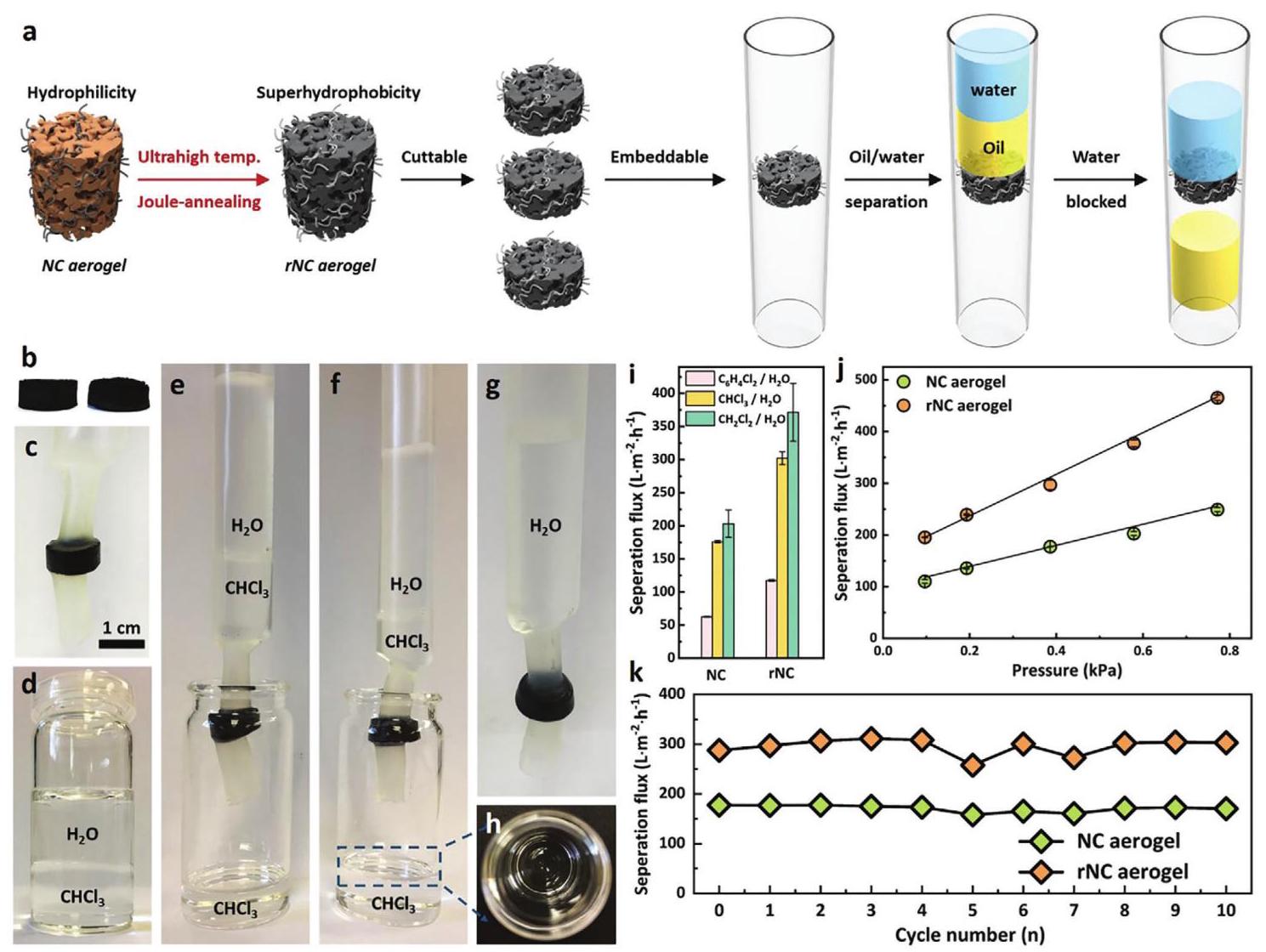
图4展示了rNC气凝胶在油水分离中的实际应用。快速电还原能够调节NC气凝胶的疏水性,这取决于电功率输入和相应的还原温度。在3000K下还原60秒的rNC气凝胶表现出超疏水性(θ=150°),结合对有机溶剂的 impressive 吸收能力,被应用于气凝胶膜分离系统。当测试氯仿-水模型混合物时,发生了快速有效的分离,展示了其在重力下进行大规模体积过滤的潜力。在升高压力下,分离通量增加(在0.8kPa下为475Lm⁻²h⁻¹,初始为200Lm⁻²h⁻¹),证实了气凝胶的机械强度。与其他混合物(二氯甲烷和1,4-二氯苯)也观察到类似的分离性能,突出了rNC气凝胶的功能能力、可靠的分离可重复性和 robust 的机械强度。
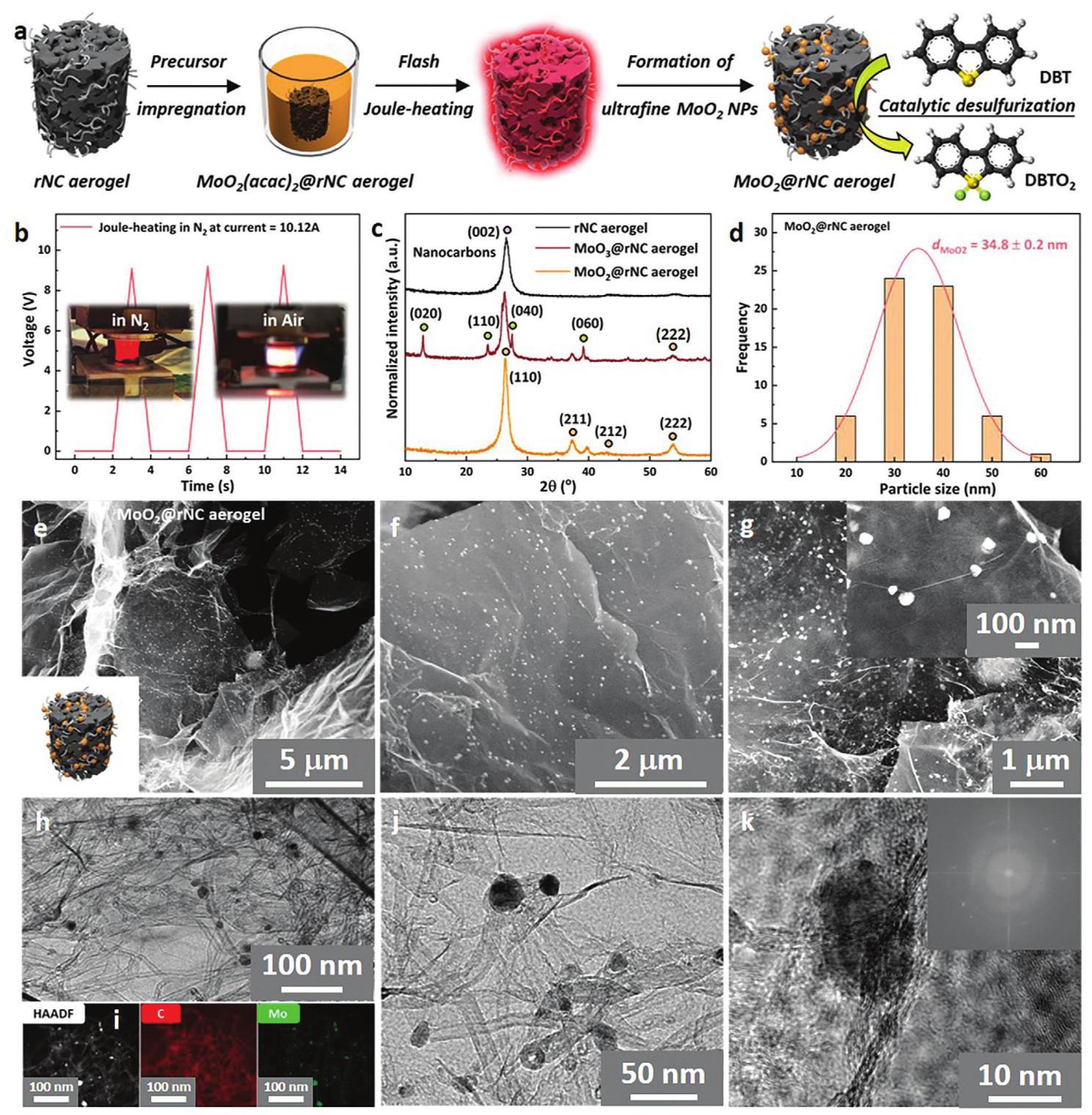
图5展示了MoO2@rNC气凝胶催化剂的制备过程和表征结果。导电气凝胶的快速加热和冷却能力被用于制备具有嵌入功能无机纳米粒子的混合NC气凝胶。rNC气凝胶通过简单的溶液相浸渍方法使用MoO2(acac)2作为前体进行修饰。通过电加热 shock-分解(在约2000K下3秒)选择性形成二氧化钼纳米粒子(Mo(IV)O2)(在氮气中)或三氧化钼纳米粒子(Mo(VI)O3)(在空气中),没有可见的气凝胶收缩。shock-分解过程促进了尺寸良好的MoO2纳米粒子在整个NC表面的均匀分布,平均粒径为34.8nm。这些MoO2纳米粒子在单斜晶相中表现出结晶度,通过TEM图像和傅里叶变换光谱中的电子散射以及XRD图谱确认。采用高角度环形暗场成像(HAADF)、能量色散X射线(EDX)光谱映射和XPS光谱进行元素组成验证。
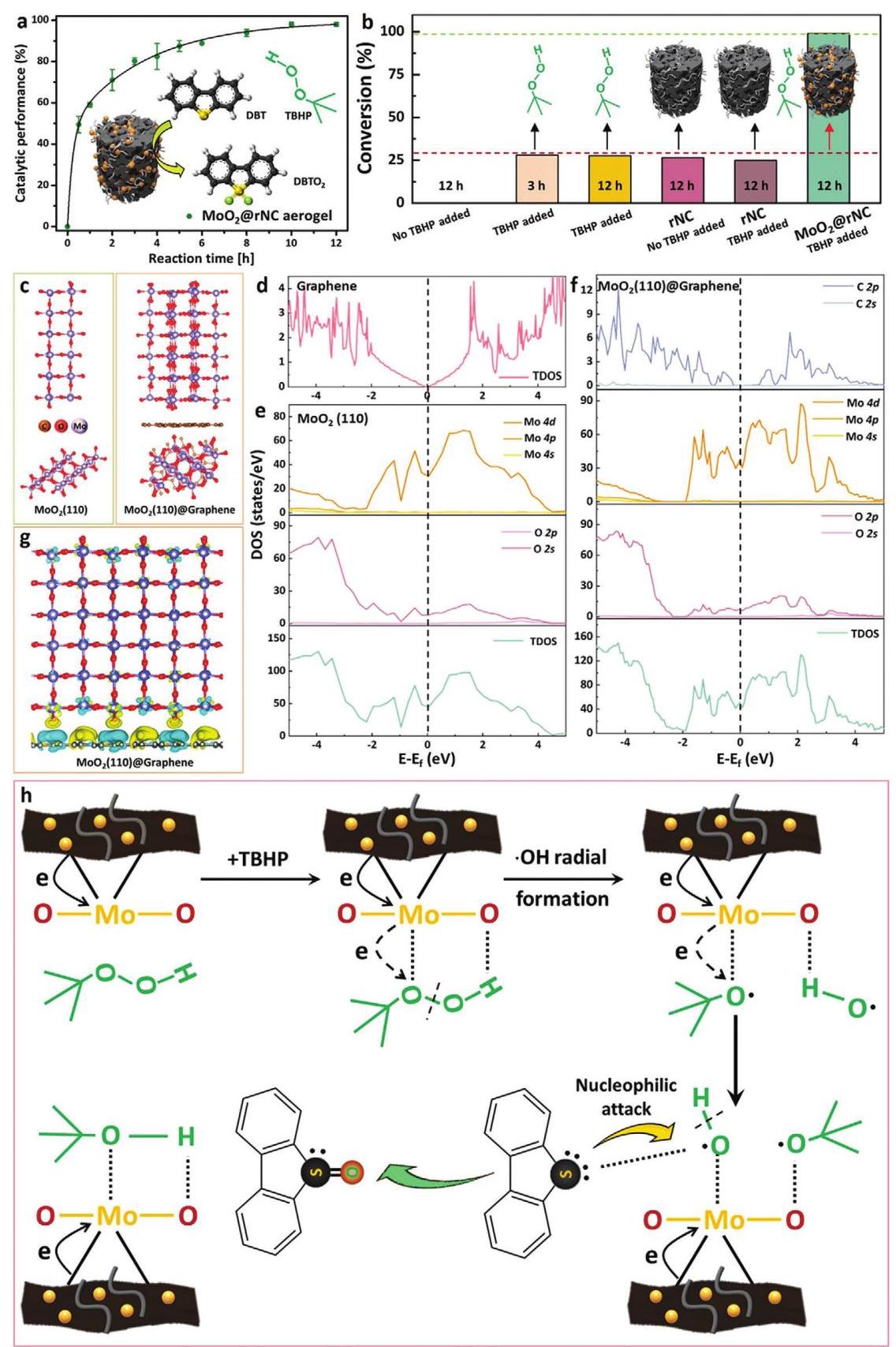
图6展示了MoO2@rNC气凝胶的催化性能和相关DFT计算结果。二苯并噻吩(DBT,燃料中常见的有机硫化合物)的催化氧化脱硫作为MoO2@rNC气凝胶的测试案例。有机硫化合物氧化转化为砜由于极性增加而实现更好的分离,对于减轻运输燃料中含硫化合物相关的环境问题(即酸雨形成)至关重要。DBT被有效转化为二苯并噻吩5,5-二氧化物(DBTO2),由负载的MoO2纳米粒子催化,并在10小时内表现出显著的催化性能,DBT转化为DBTO2的转化率达到98.9%。如此卓越的性能归因于纳米碳表面上均匀密集分布的闪速合成MoO2纳米粒子,导致暴露更多用于DBT转化的活性位点。
通过密度泛函理论(DFT)计算验证了上述假设并阐明了负载型MoO2催化剂的催化机制。石墨烯、MoO2(110)和石墨烯负载的MoO2(110)(MoO2(110)@石墨烯)的态密度(DOS)在环境温度下通过DFT计算评估。石墨烯的总态密度(TDOS)揭示了零带隙半金属的众所周知的行为。同时,MoO2的导带来自Mo4d和O2p轨道的贡献,产生重叠的价带和导带(即金属性)。MoO2(110)@石墨烯的金属性表现出显著增加,表现为Mo和O原子沿费米能级的部分态密度(PDOS)下移。这种位移表明从石墨烯到Mo和O原子的深刻电子转移。电子转移进一步通过电荷密度差异谱确认,证实了从石墨烯到金属氧化物的 considerable 电子转移,从而导致具有更高电子密度的活性Mo物种的存在,进而具有高活性。