Joule Heating-Driven \( sp^{2} \)-C Domains Modulation in Biomass Carbon for High-Performance Bifunctional Oxygen Electrocatalysis
基于焦耳加热驱动的生物质碳中 \( sp^{2} \)-C 域调制用于高性能双功能氧电催化
论文亮点
- 闪光焦耳加热可控制地增强了各种氮掺杂天然生物质基碳中的 \( sp^{2} \)-域含量。
- \( sp^{2} \)-C 域的轴向调制降低了吡啶氮和石墨氮构型的电荷密度,从而实现了出色的氧电催化性能。
研究背景
- 金属自由碳材料在电催化中具有广泛应用,但催化性能仍不理想,限制其工业应用。
- 高性能碳催化剂的设计依赖于活性位点的局部电子环境、石墨化程度和孔结构的合理调控。
- 生物质衍生碳催化剂因其低生产成本和固有多孔结构而具有吸引力,但 \( sp^{2} \)-C 域的作用尚未充分探索。
研究方法
- 使用商业椰子壳衍生活性炭(AC)作为催化剂模型。
- 通过混合2,6-二氨基吡啶/NaCl/ZnCl₂并在1000°C下退火2小时引入氮掺杂剂和结构缺陷,得到N-C₃′催化剂。
- 使用闪光焦耳加热设备在Ar气氛中以800°C/s的速率处理1秒,得到最终催化剂N-C₃。
- 制备对照样品:纯C(无添加物)、纯C₃(无氮掺杂)和N-C(无NaCl/ZnCl₂)。
- 材料表征使用HR-TEM、XPS、XRD、Raman、BET等方法。
- 电化学表征使用三电极系统测试ORR和OER性能。
- DFT计算使用VASP软件包研究反应机制。
- 组装锌-空气电池测试实际应用性能。
主要结论
- 通过闪光焦耳加热增强了 \( sp^{2} \)-C 域,优化了氮构型的电子结构,提高了催化活性。
- 催化剂在ORR中表现出半波电位0.884 V vs. RHE,与商业Pt/C相当,且具有更高的动力学电流密度。
- 在Zn-空气电池中表现出超过1200小时的循环稳定性,峰值功率密度为121 mW cm⁻²,超过商业催化剂。
结果与讨论
图1: N-C₃的合成和结构表征
图1: (a) N-C₃合成示意图; (b) N-C₃′的HR-TEM图像; (c) N-C₃的ACTEM图像; (d) (c)中红色区域的放大图像,黄色线区域表示具有规则六边形结构的 \( sp^{2} \)-C域(插图是(c)中黄色区域的FFT图案)
内容与分析:图1展示了N-C₃催化剂的合成过程和结构特征。通过闪光焦耳加热处理,N-C₃′催化剂的有序晶格条纹密度增加,表明 \( sp^{2} \)-C域含量增强。ACTEM图像显示形成了许多规则六边形区域,并增强了(002)快速傅里叶变换(FFT)图案,表明石墨化程度提高。这与控制样品中保持的无定形碳结构形成对比,证明了闪光焦耳加热在增强 \( sp^{2} \)-C域方面的有效性。
图2: 结构表征
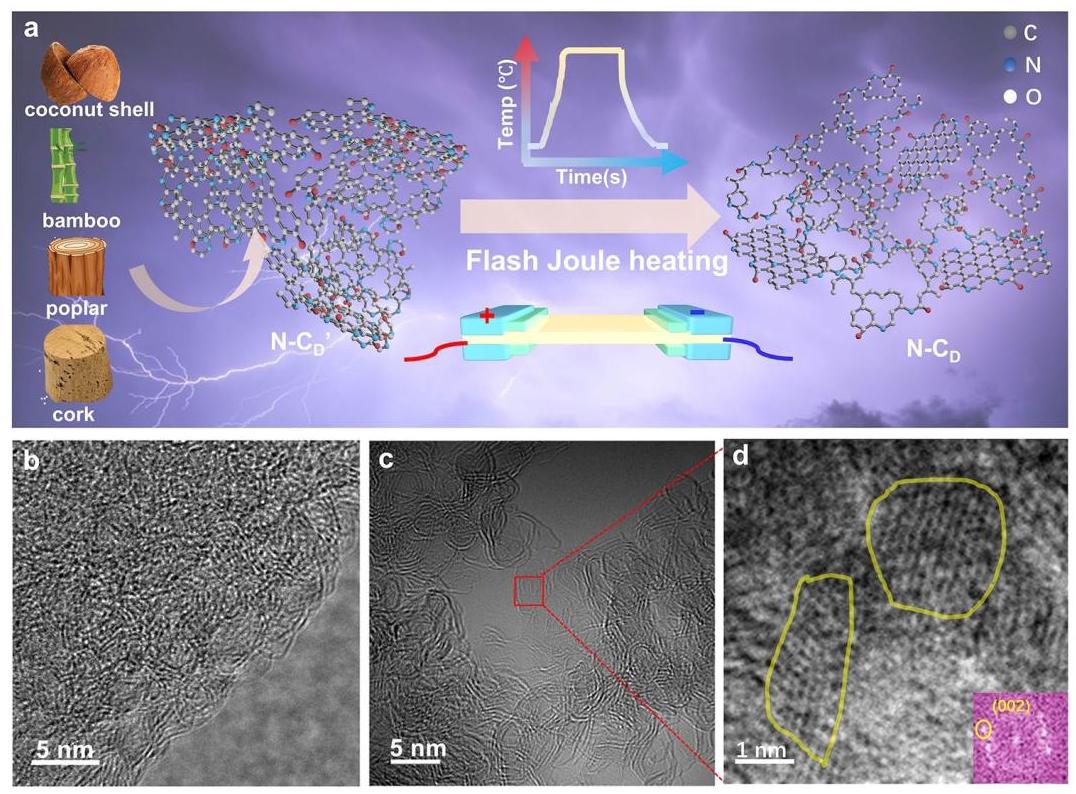
图2: (a-c) 纯C、纯C₃、N-C和N-C₃的N₂吸附-脱附等温线、XRD图谱和拉曼光谱; (d-f) N-C₃′和N-C₃的C K-edge XANES谱、高分辨率XPS C 1s谱和N 1s谱; (g) 不同样品的EPR信号
内容与分析:图2展示了各种催化剂的详细结构表征。XRD分析显示N-C₃的(002)峰强度显著增加,相应的2θ角移至23.2°,表明石墨化程度和结晶度提高。拉曼光谱显示N-C₃具有较低的D₁/G比(2.38)和较高的D₃/G比(0.41),表明石墨化程度更高且几何碳缺陷/氮掺杂剂密度增加。XPS和XANES分析证实了 \( sp^{2} \)-C构型的增强和氮构型电子环境的变化。EPR谱提供了电子环境的额外见解,显示N-C₃具有更宽更强的EPR信号,表明闪光焦耳加热处理诱导的N构型和局部 \( sp^{2} \)-C域的协同效应。
图3: 电催化性能
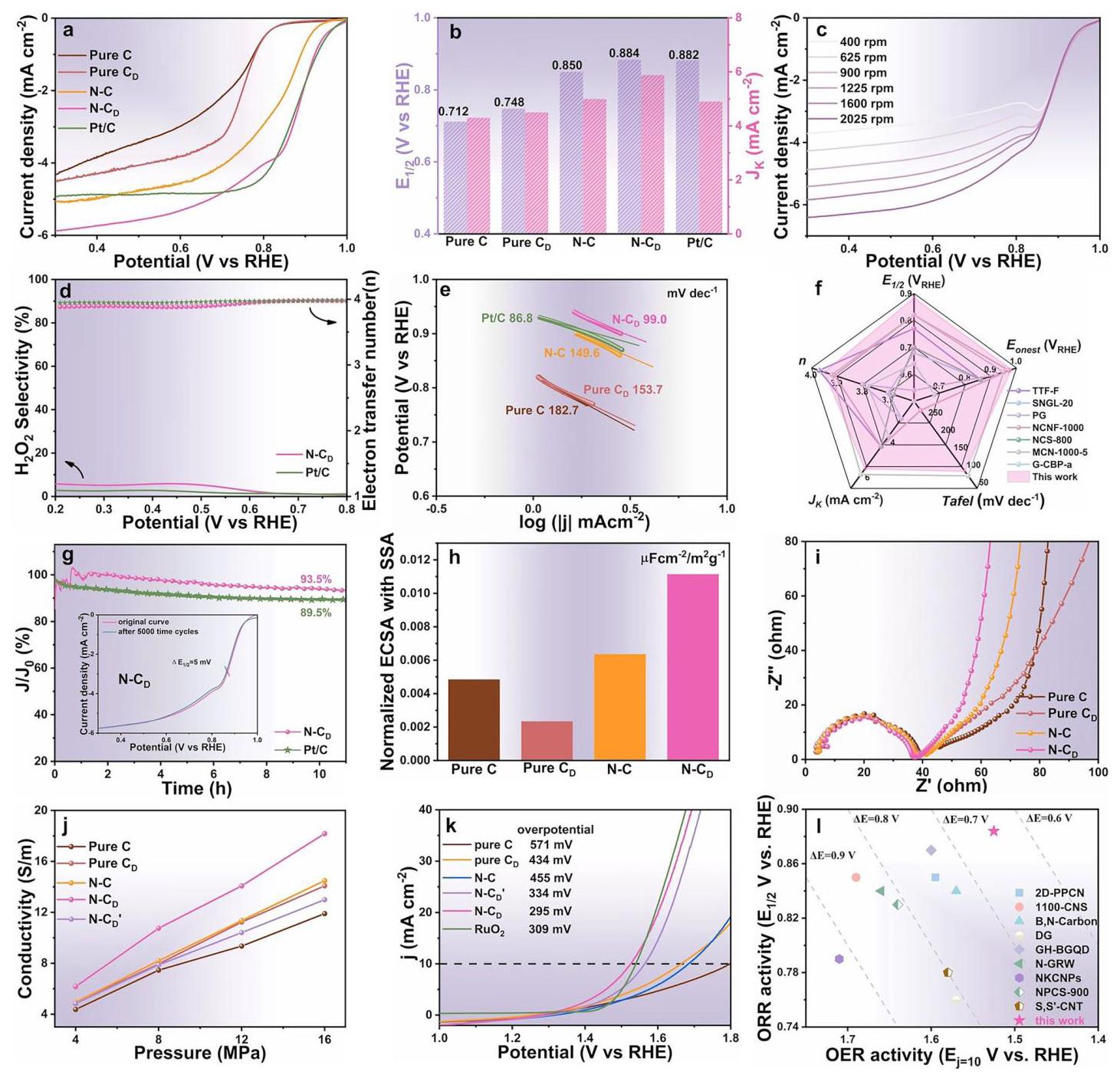
图3: (a) 在O₂饱和的0.1 M KOH中,碳催化剂和20% Pt/C在1600 rpm下的LSV曲线; (b) 不同样品的E₁/₂和Jₖ; (c) N-C₃在不同转速下的LSV曲线; (d) 用RRDE测量的N-C₃和20% Pt/C的电子转移数(虚线)和过氧化物产率(H₂O₂%,实线); (e) 基于LSV曲线的Tafel斜率; (f) 与报道催化剂的ORR性能比较雷达图; (g) N-C₃在O₂饱和的0.1 M KOH中的长期计时电流测试(插图,连续5000次CV扫描); (h) 不同样品的归一化ECSA值; (i,j) EIS谱和不同压力下的电导率图; (k) 碳催化剂和商业RuO₂催化剂在1.0 M KOH中的OER LSV曲线; (l) 与许多报道的ORR-OER双功能催化剂的催化性能比较
内容与分析:图3全面展示了N-C₃催化剂的电催化性能。在ORR测试中,N-C₃的半波电位(E₁/₂)达到0.884 V vs. RHE,与商业20% Pt/C催化剂(0.882 V vs. RHE)相当,且具有更高的动力学电流密度(5.88 mA cm⁻²)。电子转移数(n)高于3.9,表明几乎完全的4电子还原路径。N-C₃还表现出优异的催化稳定性,11小时后保留93.5%的初始电流密度,5000次CV循环后E₁/₂仅降低5mV。在OER测试中,N-C₃在10 mA cm⁻²下的过电位为295mV,低于商业RuO₂催化剂(309mV)。双功能性能通过ΔE(Ej=10 - E₁/₂)评估,N-C₃的ΔE仅为0.64V,远低于大多数报道的金属自由双功能电催化剂。
图4: \( sp^{2} \)-C域的形成机制
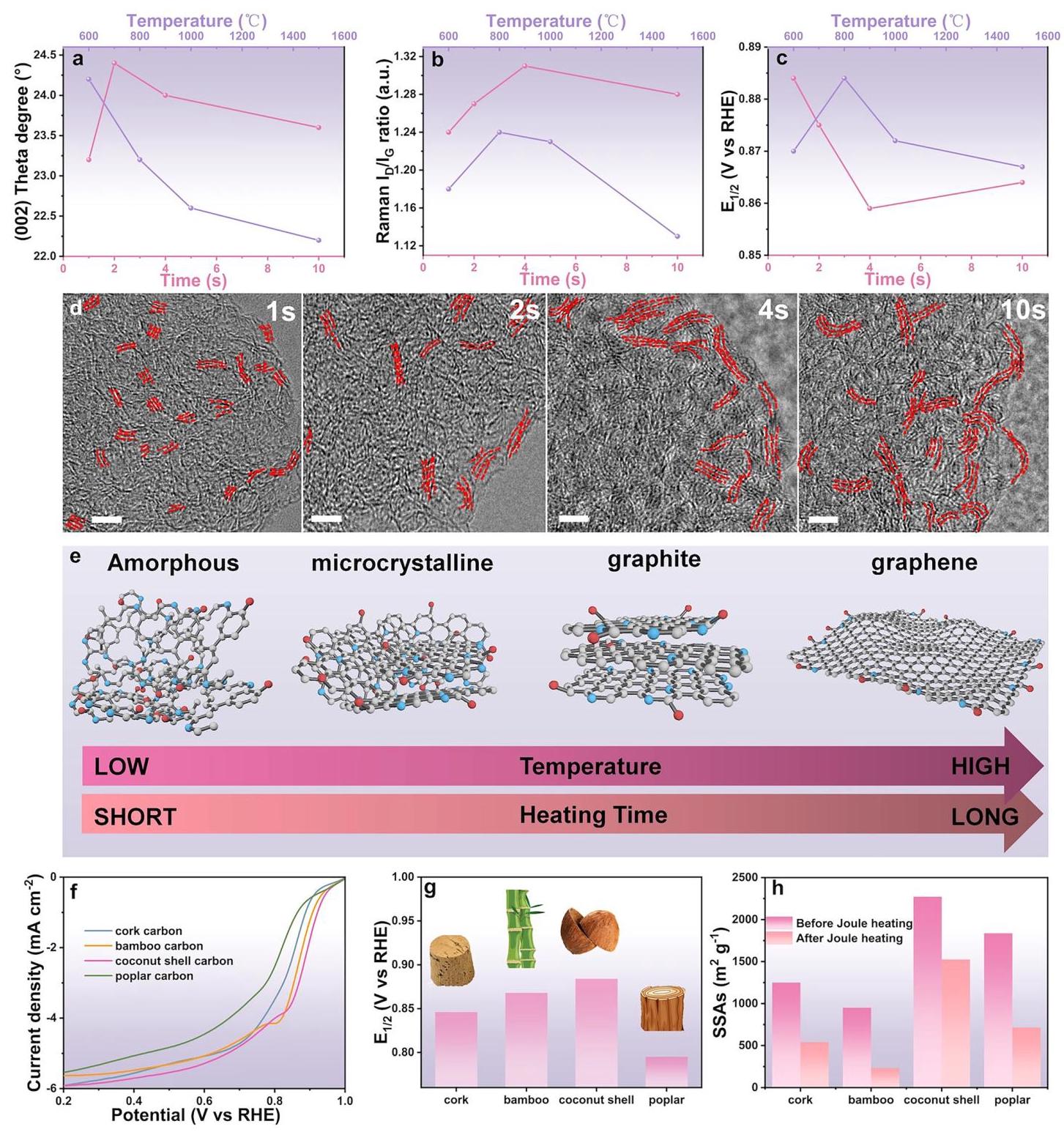
图4: (a-c) 焦耳加热时间和温度对XRD图案中(002)平面的2θ角度、拉曼光谱中的I_D/I_G比和ORR性能的影响; (d) 不同焦耳加热时间(1至10秒)下N-C₃的HR-TEM图像; (e) 随着焦耳加热时间延长和加热温度升高,碳纳米结构的示意图; (f,g) 不同天然生物质基碳催化剂在O₂饱和的0.1 M KOH电解质中的LSV曲线和起始电位; (h) 在800°C下焦耳加热1秒前后SSAs的变化
内容与分析:图4研究了 \( sp^{2} \)-C域的形成机制及其对催化性能的影响。随着加热速率增加(800-1500°C/1s),(002)面的2θ角度减小,表明层间距增加,同时I_D/I_G比逐渐降低,代表活性位点密度减少。通过平衡 \( sp^{2} \)-C域和活性位点密度,确定了优化的闪光焦耳加热条件(800°C/1s),实现了最高的ORR性能。延长加热时间(1至10秒)进一步促进了类石墨烯结构的形成,2θ角度和I_D/I_G比呈现火山型趋势,表明 \( sp^{2} \)-C域首先形成较大的石墨结构,然后在快速冷却过程中剥离成类石墨烯结构。该方法还扩展到其他生物质基活性炭,均显著增强了 \( sp^{2} \)-C域并改善了ORR性能。
图5: 机制分析
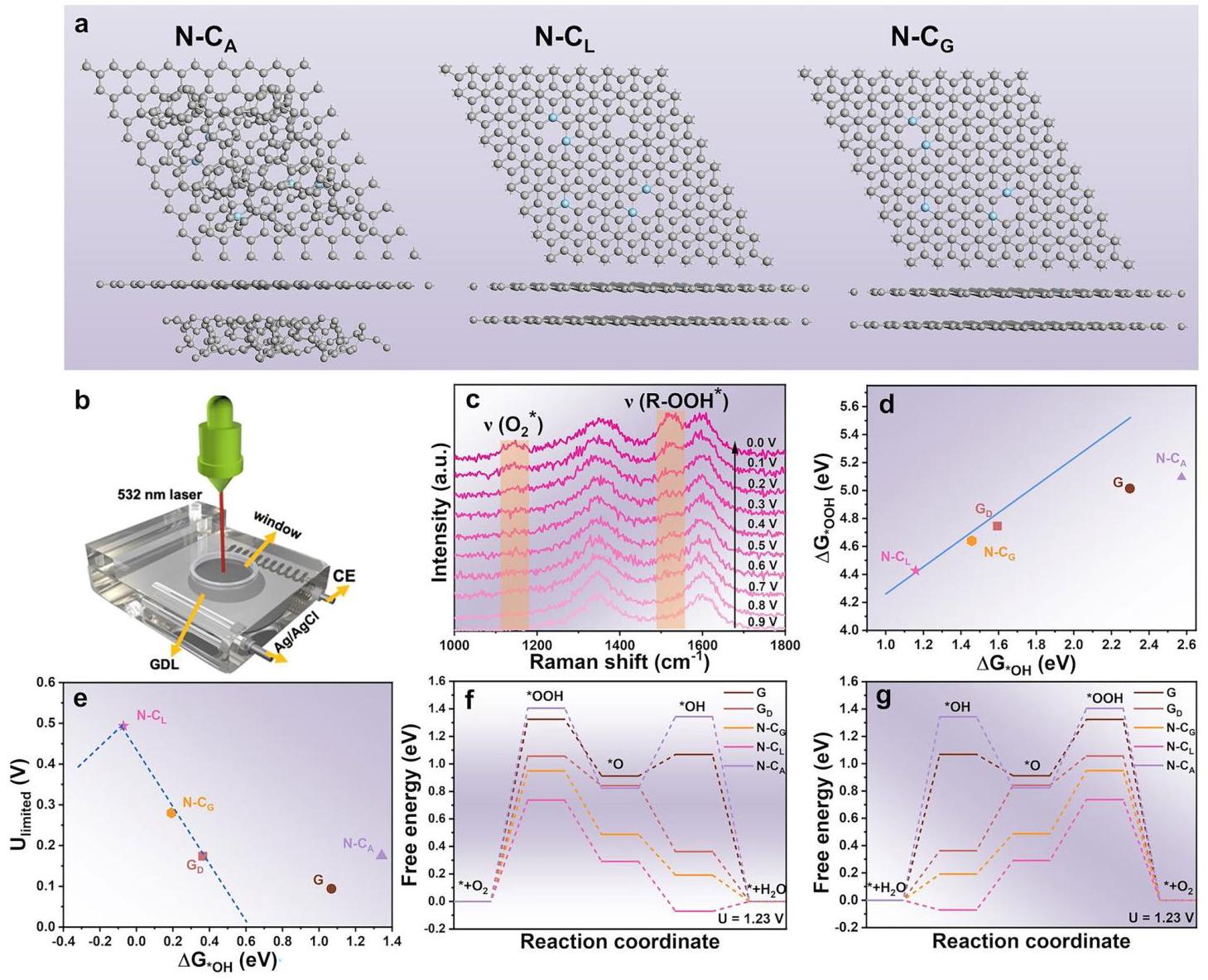
图5: (a) N-C_A、N-C_L、N-C_G的DFT计算模型; (b) 测量原位拉曼光谱的设置; (c) 在0.1 M KOH中,N-C₃上*OOH中间体在不同电位下的原位拉曼光谱研究; (d) ΔG*OOH和ΔG*OH之间的缩放关系; (e) 理论起始电位与ΔG*OH的ORR火山图; (f) 不同催化剂在1.23 V下ORR中间体的吉布斯自由能; (g) 不同催化剂在1.23 V下OER中间体的吉布斯自由能
内容与分析:图5通过DFT计算和原位拉曼光谱揭示了 \( sp^{2} \)-C域增强催化活性的机制。DFT计算设计了N-C_A、N-C_L和N-C_G模型,分别代表N掺杂石墨烯层与相邻无定形碳层、局部增强 \( sp^{2} \)-C碳层或石墨烯层。原位拉曼光谱显示,随着电位从0.8降低到0 V vs. RHE,1140和1520 cm⁻¹处的信号增强,归因于O₂⁻物种的O-O伸缩振动和吸附的*OOH。N-C_L催化剂位于火山图的峰值,表明其优异的催化活性,优化的*OOH吸附能值有利于高效的ORR动力学。在OER反应路径中,N-C_L在整个OER过程中表现出最低的能垒,特别是在关键的*O到*OOH转变过程中,展示了优异的OER性能。DFT计算揭示了N掺杂和局部增强 \( sp^{2} \)-C域之间的协同作用优化了活性C位点的电子结构,从而增强了ORR和OER的催化性能。
图6: Zn-空气电池应用
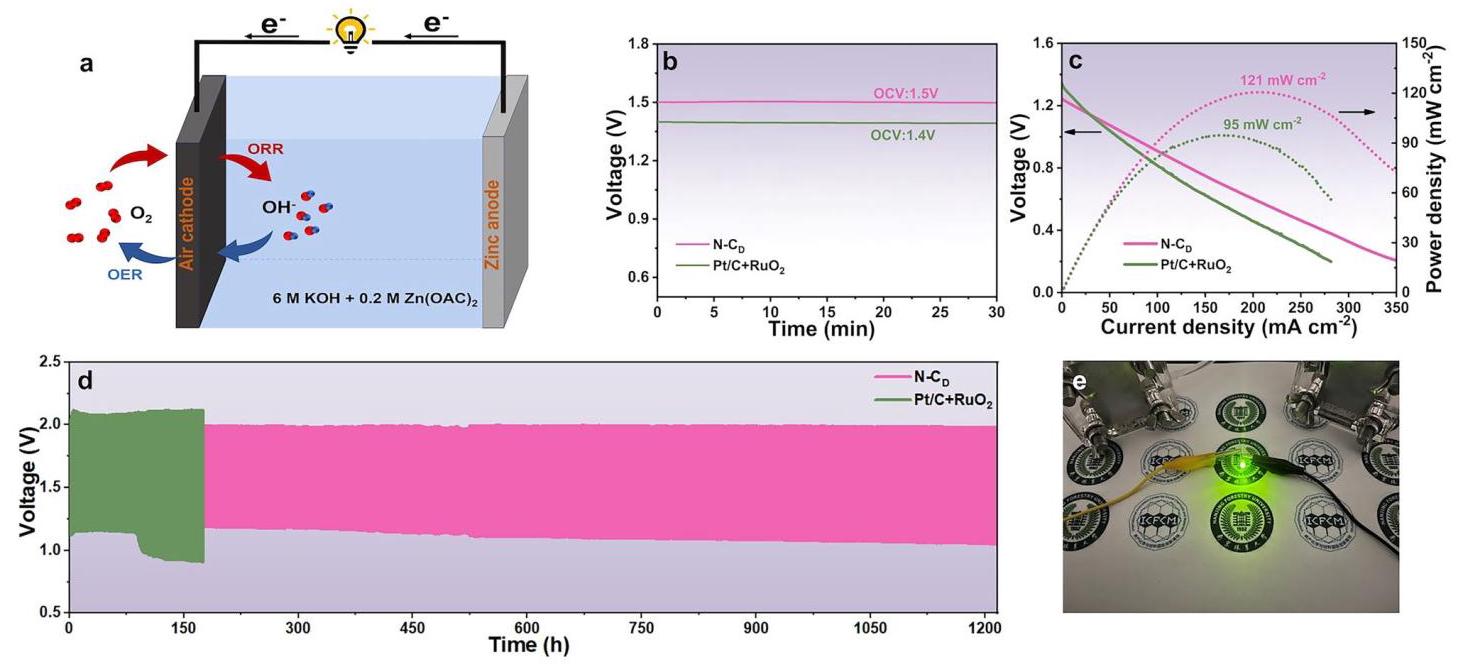
图6: (a) 组装的ZAB示意图; (b) 使用N-C₃或Pt/C+RuO₂空气阴极的ZAB的开路电压; (c) 放电极化曲线和相应的功率密度图; (d) ZAB在5 mA cm⁻²下的放电-充电循环曲线; (e) 两个N-C₃组装的ZAB供电的绿色LED照片
内容与分析:图6展示了N-C₃催化剂在锌-空气电池(ZAB)中的实际应用性能。使用N-C₃空气阴极的ZAB实现了1.5V的开路电压和121 mW cm⁻²的峰值功率密度,显著优于商业20% Pt/C+RuO₂双功能催化剂(1.4V和95 mW cm⁻²)。长期稳定性测试在5 mA cm⁻²的电流密度下进行,交替10分钟充电和放电循环。使用Pt/C+RuO₂催化剂的ZAB在80小时后电位间隙增加0.18V,而