催化剂合成与表征

图1. Ni@NC20/Ni电化学CO2还原示意图
该示意图展示了Ni@NC20/Ni电子库单原子电催化剂的CO2电还原过程。碳包覆的Ni纳米颗粒作为电子库,将电子定向传递到周围的Ni-N4单原子活性位点,促进CO2分子的活化和还原。
Wanli Yia, Changsheng Houa, Renyi Lia, Yinji Wanb, Xuan Zhanga, Bing Mac, Wenchao Hua, Shenghui Hana, Mulin Qina, Limeng Sunb, Qian Wanga,*, Yonggang Wanga,*, Xiao Haia,*, Ruqiang Zoua,*
a 北京大学材料科学与工程学院,北京 100871,中国
b 中国石油大学(北京)重质油国家重点实验室,北京 102249,中国
c 郑州大学化学学院晶体分子功能材料河南省重点实验室,郑州 450001,中国
采用二次负载法结合快速热冲击技术合成混合电催化剂Ni@NC20/Ni:

图1. Ni@NC20/Ni电化学CO2还原示意图
该示意图展示了Ni@NC20/Ni电子库单原子电催化剂的CO2电还原过程。碳包覆的Ni纳米颗粒作为电子库,将电子定向传递到周围的Ni-N4单原子活性位点,促进CO2分子的活化和还原。
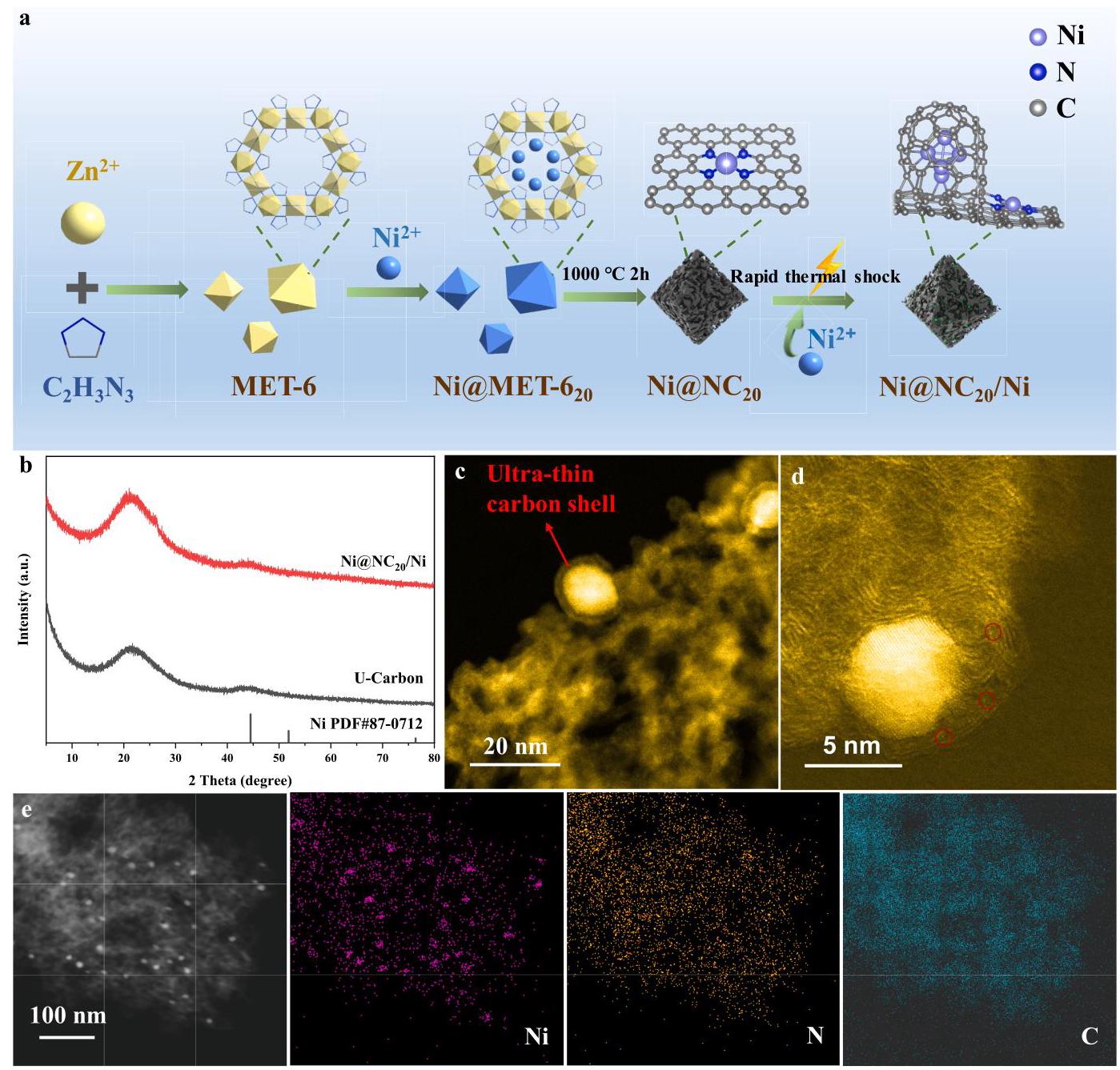
图1. 制备催化剂的合成与表征。(a) Ni@NC20和Ni@NC20/Ni催化剂的合成示意图。(b) Ni@NC20/Ni催化剂的XRD图谱。(c,d) Ni@NC20/Ni催化剂的HAADF-STEM图像。(e) Ni@NC20/Ni催化剂的暗场透射电子显微镜图像和相应的EDS mapping
XRD分析显示Ni@NC20/Ni催化剂具有无定形碳的特征宽峰,未观察到明显的Ni晶体衍射峰,表明Ni主要以单原子或小纳米颗粒形式存在。HAADF-STEM图像显示所有Ni纳米颗粒都被超薄碳层包裹,碳载体上Ni纳米颗粒周围观察到大量Ni单原子亮点。EDS mapping进一步验证了Ni单原子和Ni纳米颗粒在Ni@NC20/Ni催化剂中的均匀分布。
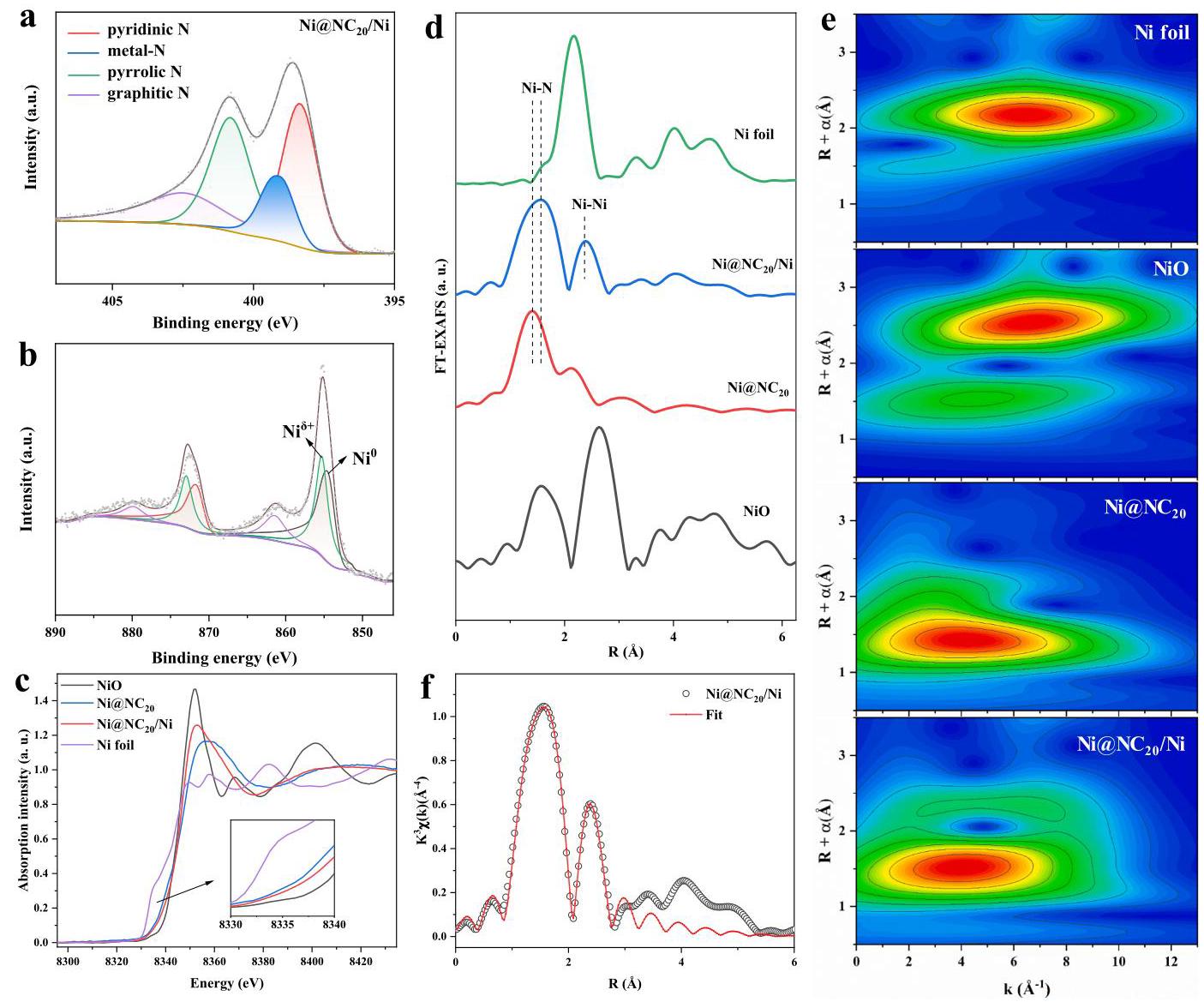
图2. X射线光电子能谱和X射线吸收光谱分析。(a) Ni@NC20/Ni催化剂的N 1s和(b) Ni 2p谱。(c) Ni@NC20和Ni@NC20/Ni催化剂在Ni K-edge的XANES和(d) FT-EXAFS谱。(e) Ni箔、NiO、Ni@NC20和Ni@NC20/Ni的WT-EXAFS等高线图。(f) Ni@NC20/Ni催化剂的FT-EXAFS拟合结果
XPS分析显示Ni@NC20/Ni催化剂中Ni0和Niδ+物种共存。XANES表明Ni物种的平均价态介于0和+2之间。FT-EXAFS谱显示在约1.4Å和2.4Å处有两个主峰,分别归因于Ni-N和Ni-Ni散射路径,表明单原子Ni-Nx位点和Ni纳米颗粒共存。EXAFS曲线拟合分析表明Ni@NC20/Ni催化剂中Ni-N配位数约为3.77,Ni-Ni配位数约为6.13。
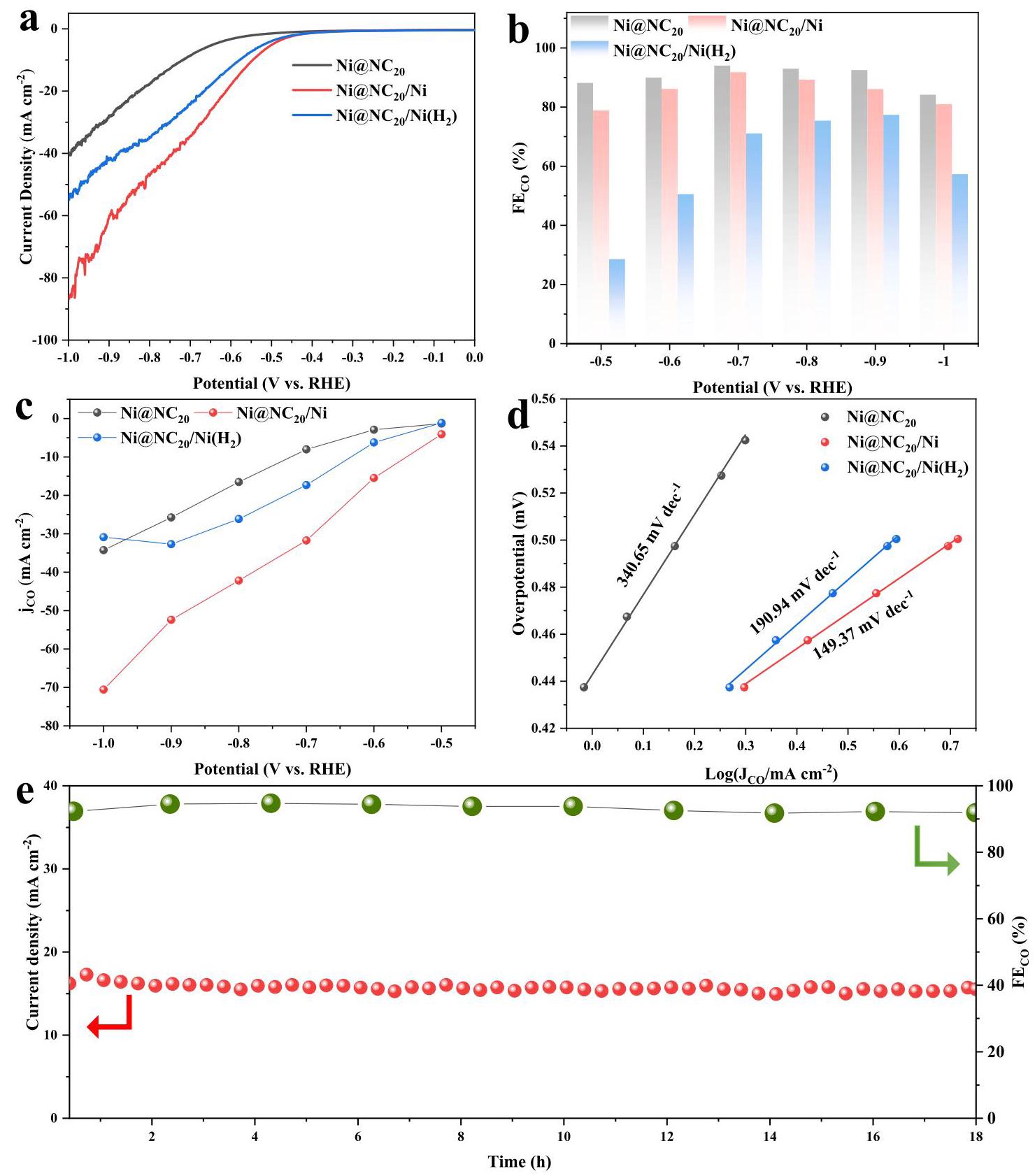
图3. CO2电还原性能。(a) LSV曲线,(b) 法拉第效率,(c) CO部分电流密度和(d) Ni@NC20、Ni@NC20/Ni和Ni@NC20/Ni(H2)催化剂在CO2饱和的0.5M KHCO3中的Tafel图。(e) Ni@NC20/Ni催化剂在CO2饱和的0.5M KHCO3中于恒定电位-0.7V下的耐久性测试
Ni@NC20/Ni表现出最高的CO生成选择性,在-0.7V vs. RHE条件下CO法拉第效率达到93%,在-0.6V至-0.9V电位范围内保持超过86%。在-0.7V vs. RHE条件下,Ni@NC20/Ni实现了31.7 mA cm-2的显著CO部分电流密度,比Ni@NC20/Ni(H2)高1.8倍,比Ni@NC20高4.0倍。Ni@NC20/Ni电催化剂的Tafel斜率为149.37 mV dec-1,远低于Ni@NC20/Ni(H2)和Ni@NC20,表明其具有更快的CO生成动力学。
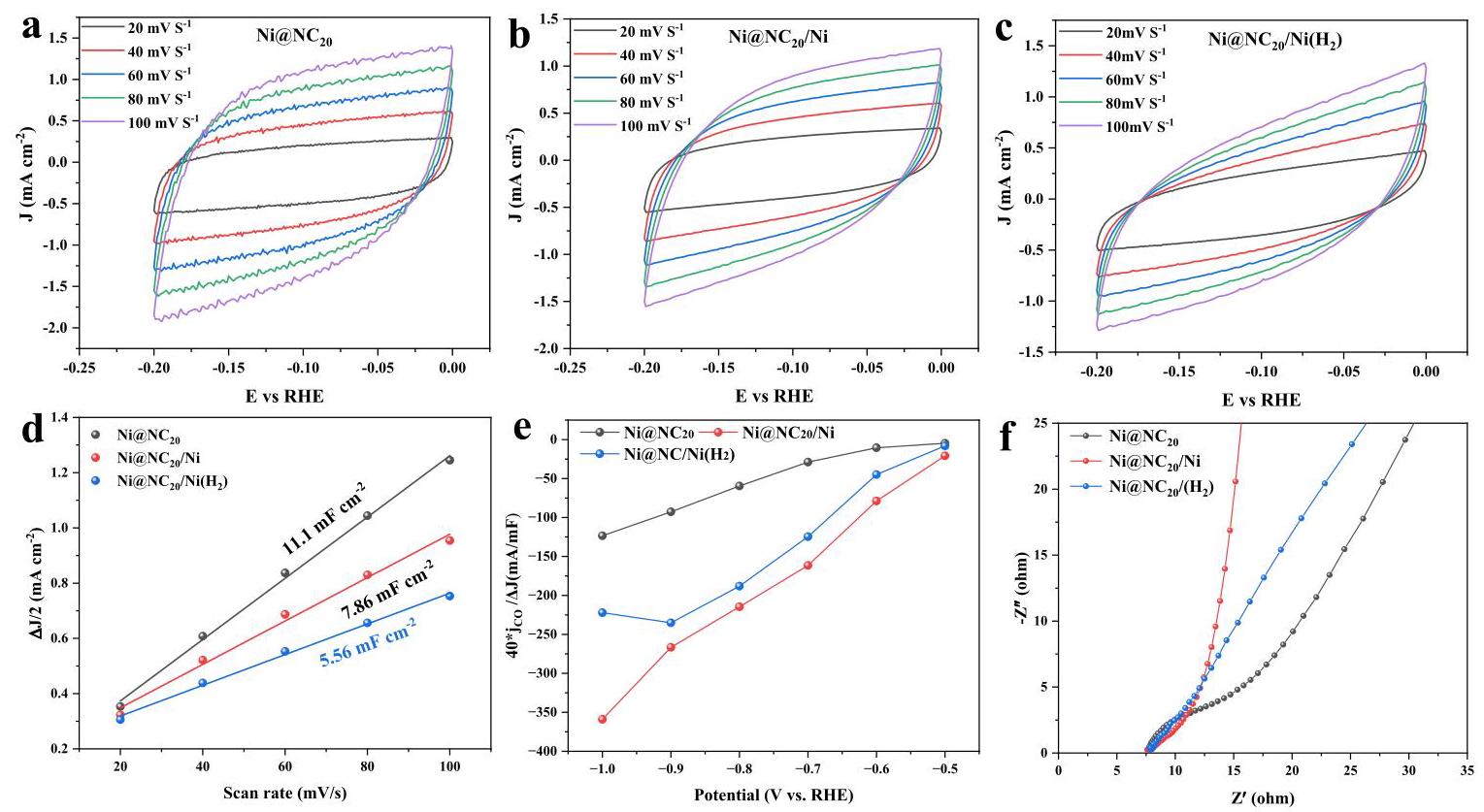
图4. CO2电还原性能。(a-c) 不同扫描速率(20-100mV)下的循环伏安曲线,(d) 电容电流密度差的一半随扫描速率的变化,(e) 样品的本征活性(样品的CO部分电流密度除以活性面积)和(f) Ni@NC20、Ni@NC20/Ni和Ni@NC20/Ni(H2)催化剂在CO2饱和的0.5M KHCO3中的Nyquist图(在开路电压下测量)
电化学活性表面积(ECSA)估算表明,Ni@NC20/Ni的改进ECR活性主要归因于其本征催化活性而非表面积的增加。电化学阻抗谱(EIS)测试显示,与Ni@NC20和Ni@NC20/Ni(H2)相比,Ni@NC20/Ni具有最低的电荷转移电阻,表明碳包覆Ni纳米颗粒促进了电荷转移过程,增强了电子电导率,最终提高了其ECR活性。
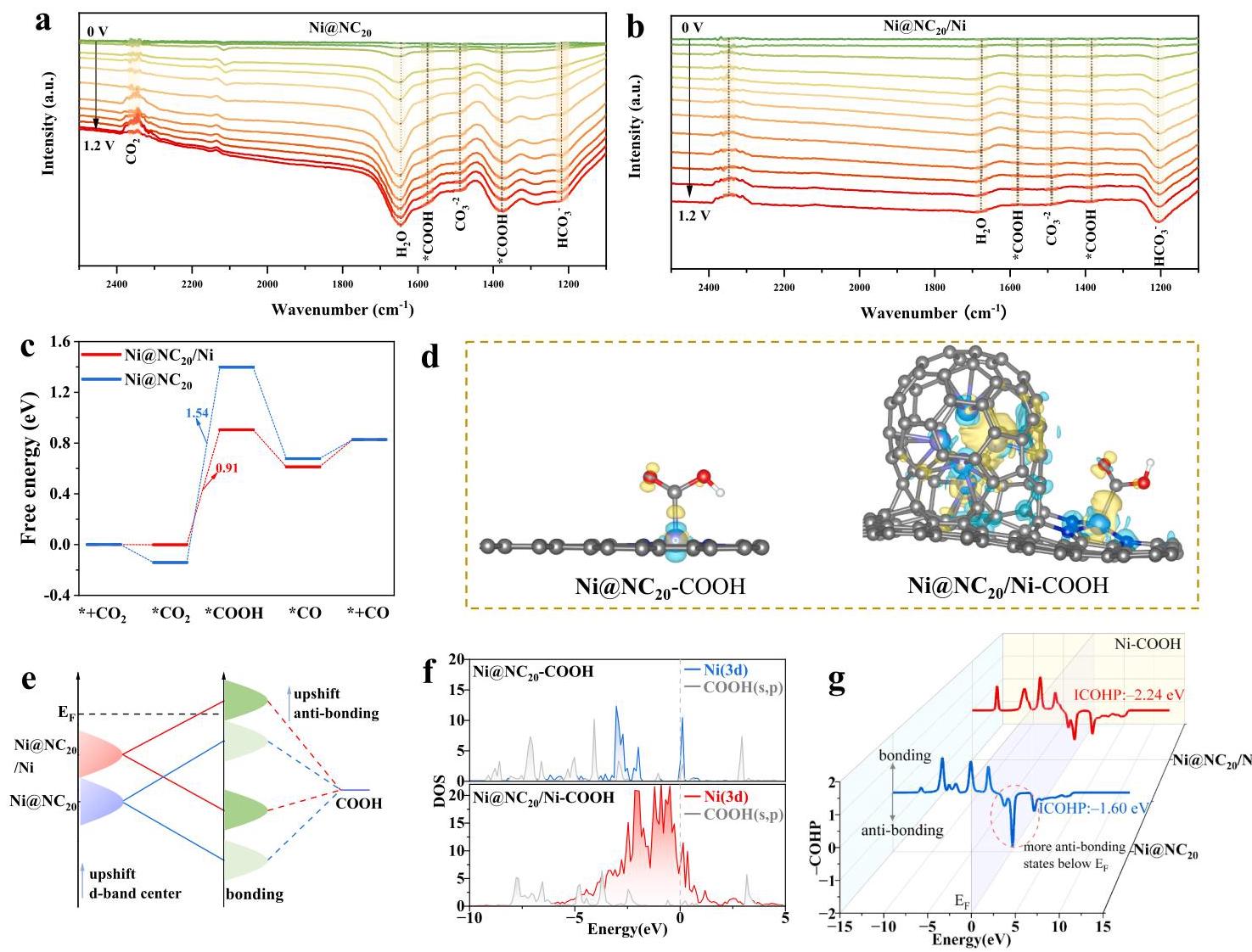
图5. (a) Ni@NC20和(b) Ni@NC20/Ni催化剂的原位ATR-SEIRAS谱。(c) Ni@NC20/Ni和Ni@NC20上ECR的自由能图。(d) *COOH中间体吸附在Ni@NC20和Ni@NC20/Ni上的电荷密度差分布。(e) 通过移动Ni的d带中心说明Ni-COOH相互作用的变化的示意图。(f) Ni@NC20-COOH和Ni@NC20/Ni-COOH的电子态密度(DOS)。(g) Ni@NC20-COOH(蓝色)和Ni@NC20/Ni-COOH(红色)中Ni-C键的晶体轨道哈密顿布居(COHP)
原位ATR-SEIRAS分析显示,在1377 cm-1和1574 cm-1处观察到的峰归属于*COOH中间体的对称和不对称C-O伸缩,这是CO2电还原为CO的关键中间体。Ni@NC20/Ni中*COOH中间体的峰强度显著降低,表明其ECR能力更快。DFT计算表明,引入碳包覆Ni纳米颗粒后,*COOH形成的自由能垒从Ni@NC20的1.54 eV降低到Ni@NC20/Ni的0.91 eV。碳包覆的Ni纳米颗粒作为碳基底上的电子库,持续向附近的Ni原子位点提供电子,促进电子转移,增强*CO2氢化为*COOH的形成能力。