图1: FeCoMnCuAl高熵合金电催化剂的合成与表征
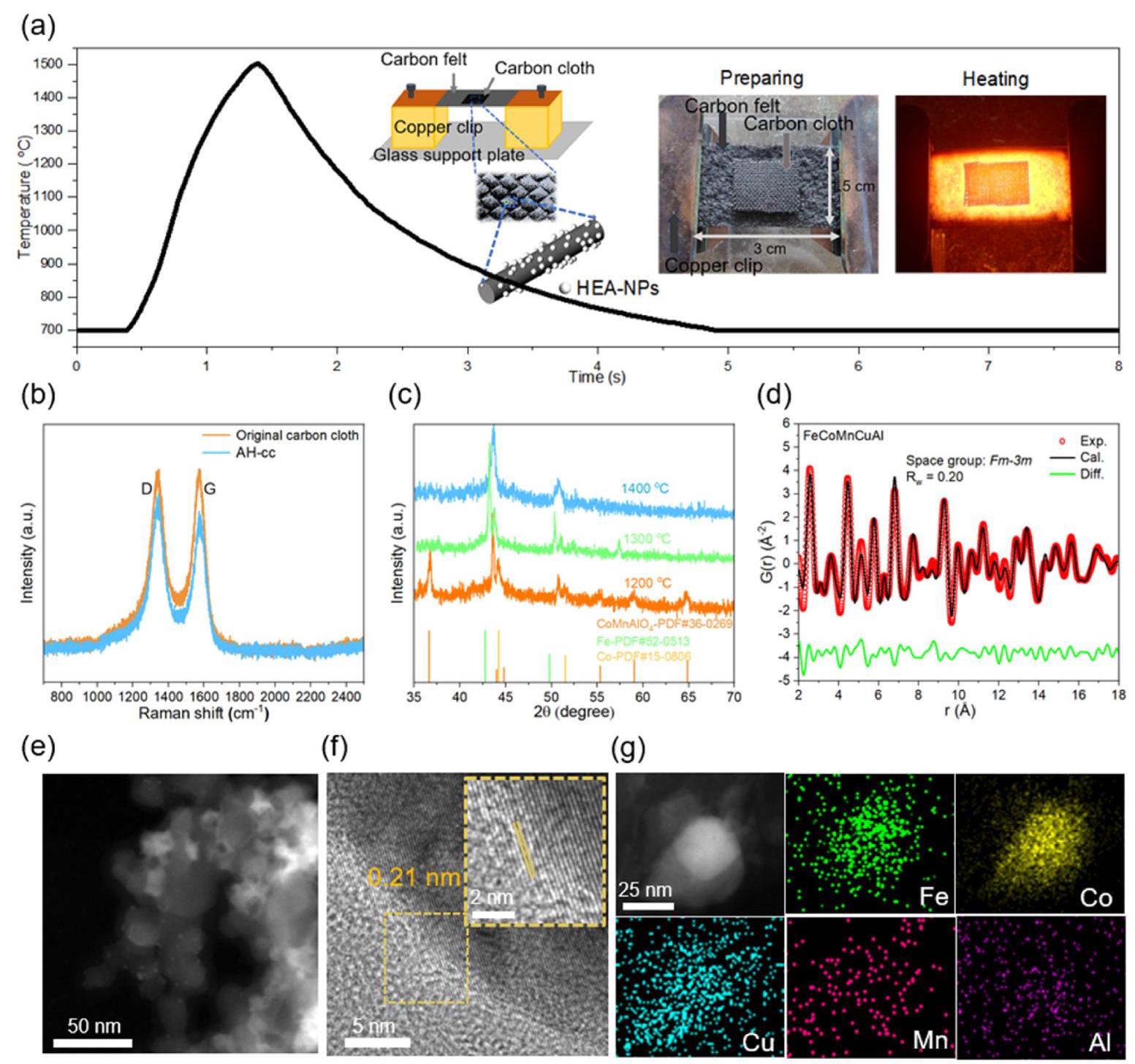
图1: (a)典型HTS合成的温度曲线,插图为FeCoMnCuAl HEA电催化剂的示意图、制备照片和样品台加热阶段;(b)原始碳布和AH-cc的拉曼光谱;(c)不同合成温度下制备的FeCoMnCuAl HEA电催化剂的XRD图谱;(d)FeCoMnCuAl HEA电催化剂的PDF图谱;(e)FeCoMnCuAl HEA NPs的TEM图像;(f)HRTEM图像;(g)FeCoMnCuAl HEA NPs的Fe、Co、Mn、Cu和Al元素分布图。
分析与结果
图1(a)展示了HTS过程的温度曲线,加热/冷却速率高达约1000°C/秒,这种超快过程抑制了相分离和原子扩散。图1(b)的拉曼光谱显示,处理后的碳布(ID/IG=1.18)比原始碳布(ID/IG=0.99)具有更高的缺陷含量,有利于HEA NPs的负载和分散。图1(c)的XRD图谱表明在1400°C下形成了单相FCC结构的HEA,晶格参数约为3.56 Å。图1(d)的PDF分析进一步证实了FCC结构,拟合的晶格参数为3.60 Å,略大于XRD结果,表明存在局部晶格畸变。图1(e-g)的TEM和元素分布图显示NPs平均尺寸约为25 nm,元素分布均匀,证实了高熵合金的形成。