合成样品的物理和形态分析

图1: (A-C)采用5个阴极的共聚焦磁控溅射配置示意图。(B)溅射薄膜样品的表面和(C)体相组成。(D-F)碳热冲击合成装置示意图和合成碳载纳米颗粒时使用的典型温度曲线。(E)碳载Pt和(F)PtRuIrRhPd样品的TEM图像。插图显示了PtRuIrRhPd样品采集的HAADF-STEM和EDX图像。
研究结果表明,两种合成方法都能制备出完美混合、均匀的复杂合金系统,且为单相结构,克服了相图中的混溶间隙。
第一作者: Attila Kormányos
通讯作者: Attila Kormányos, Serhiy Cherevko
德国埃尔朗根-纽伦堡大学、匈牙利塞格德大学、德国于利希研究中心等
DOI: 10.1016/j.isci.2023.107775
期刊: iScience
发表年份: 2023

图1: (A-C)采用5个阴极的共聚焦磁控溅射配置示意图。(B)溅射薄膜样品的表面和(C)体相组成。(D-F)碳热冲击合成装置示意图和合成碳载纳米颗粒时使用的典型温度曲线。(E)碳载Pt和(F)PtRuIrRhPd样品的TEM图像。插图显示了PtRuIrRhPd样品采集的HAADF-STEM和EDX图像。
研究结果表明,两种合成方法都能制备出完美混合、均匀的复杂合金系统,且为单相结构,克服了相图中的混溶间隙。
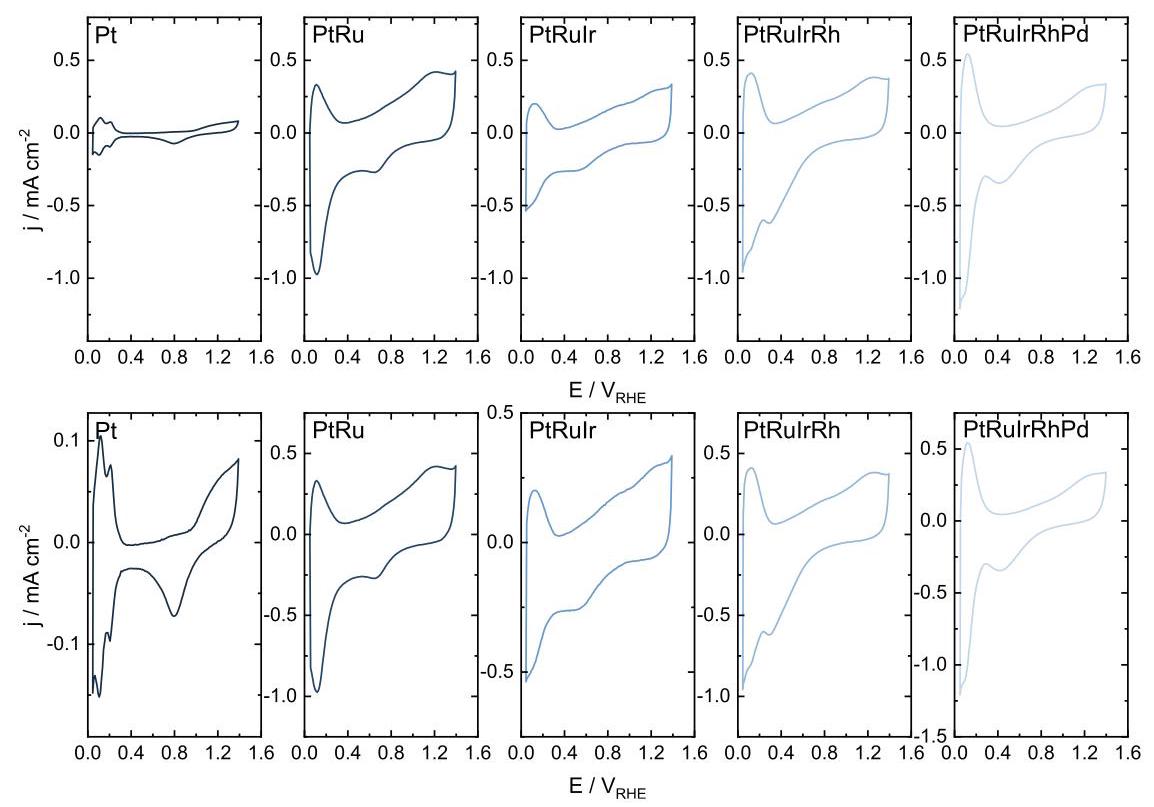
图2: 在0.1 M HClO4电解质溶液中,在0.05 VRHE和1.4 VRHE之间记录的薄膜(上行)和碳载纳米颗粒(下行)的CV曲线,扫描速率为200 mV s-1。电解质溶液用Ar饱和。
分析表明,随着合金组成元素数量的增加,CV曲线的面积显著增加,特别是在氢欠电位沉积(HUPD)区域,表明电化学活性表面积(ECSA)随着合金组成元素数量的增加而显著增加。
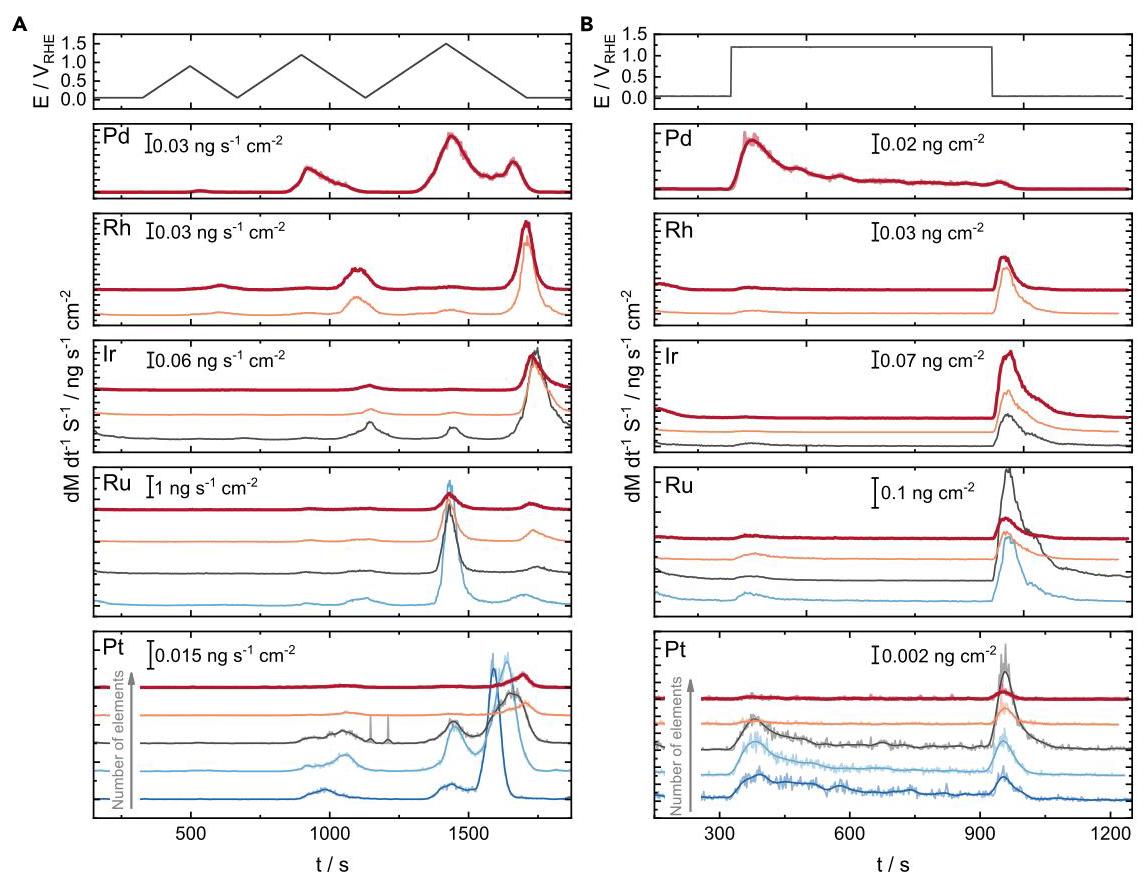
图3: (A)协议包括在0.05 VRHE下保持5分钟,然后进行三个连续CV,逐渐增加上限电位(0.9、1.2和1.5 VRHE),扫描速率为5 mV s-1。协议最后在0.05 VRHE下进行3分钟电位静态保持。(B)协议开始在0.05 VRHE下保持5分钟,然后在1.2 VRHE下额外保持10分钟。测量最后在0.05 VRHE下进行5分钟电位静态保持。
研究发现在酸性介质中,二元合金(PtRu)的Pt溶解显著增加,但当合金组成元素数量超过三个时,溶解显著减少,PtRuIrRh和PtRuIrRhPd的Pt溶解特征几乎不可见。
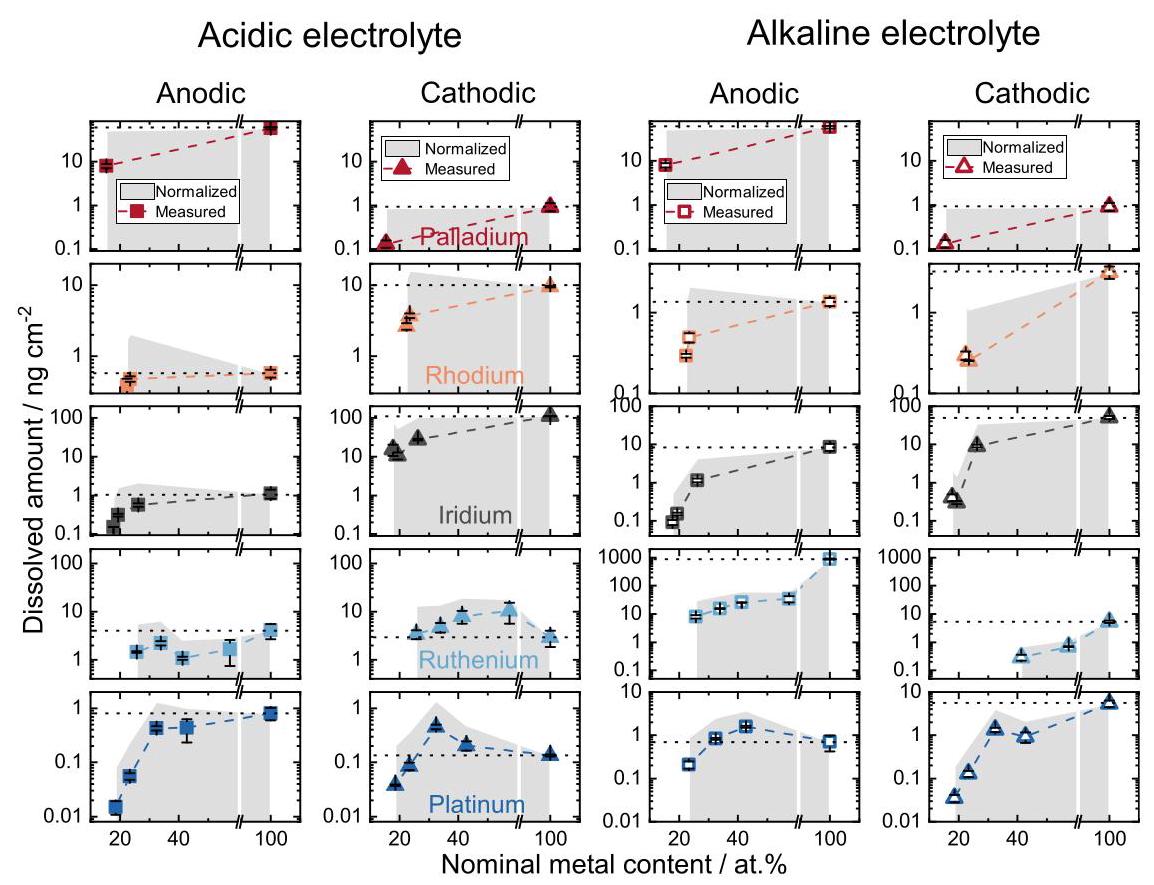
图4: 左两列(酸性,0.1 M HClO4电解质):溶解量作为给定元素在合金样品中摩尔分数的函数。右两列(碱性,0.05 M KOH电解质):溶解量作为给定元素在合金样品中摩尔分数的函数。
分析表明,在酸性介质中,阳极和阴极溶解随着合金组成元素数量的增加而减少,这主要是由于合金中所有金属的摩尔分数逐渐降低,而不是因为稳定性增强。相比之下,在碱性介质中,高熵合金样品中Pt、Ru和Ir的标准化溶解量(NDA)显著降低。
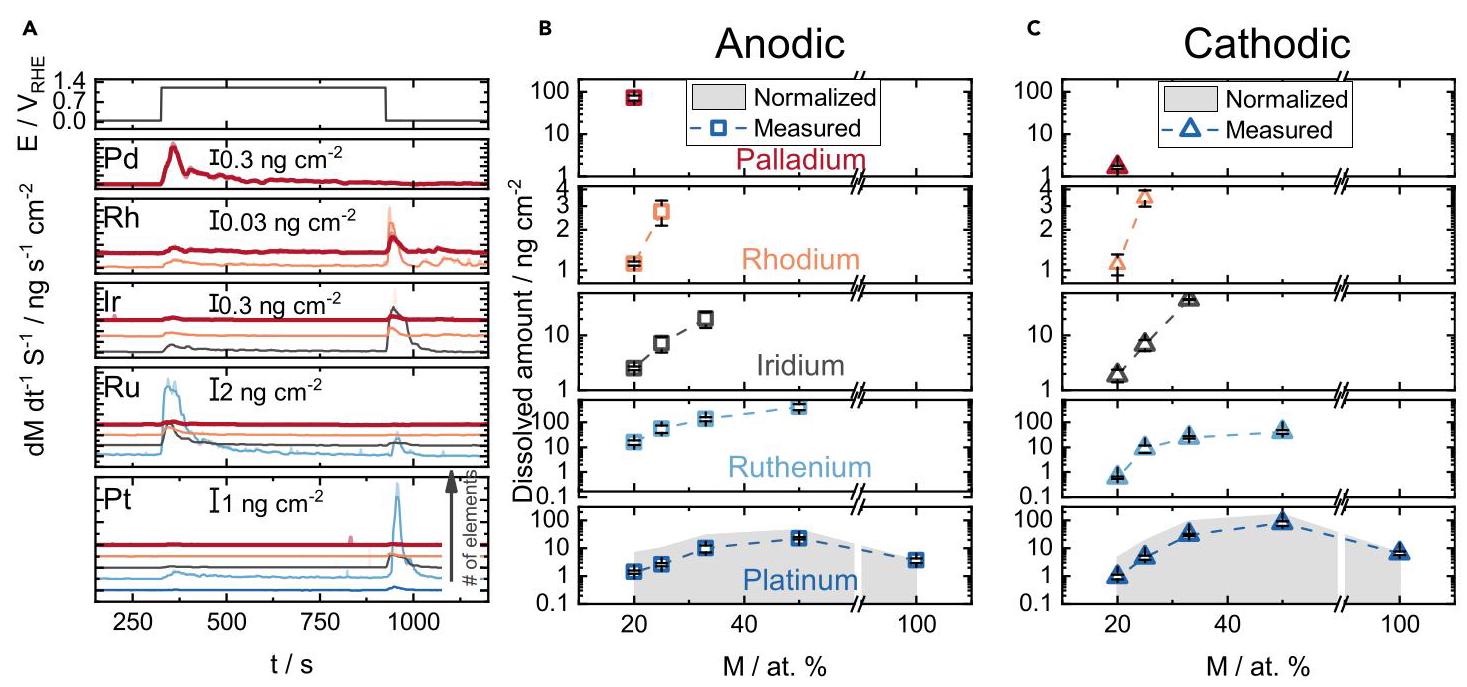
图5: (A)碳载纳米颗粒在碱性介质(0.05 M KOH)中的溶解曲线。(B,C)溶解量作为给定元素在合金样品中摩尔分数的函数。
研究发现碳载纳米颗粒系统与薄膜系统的稳定性相当,只有小的差异。纳米颗粒的溶解量遵循与薄膜相同的趋势,无论使用何种电解质,它们都与合金中给定金属的含量成比例。
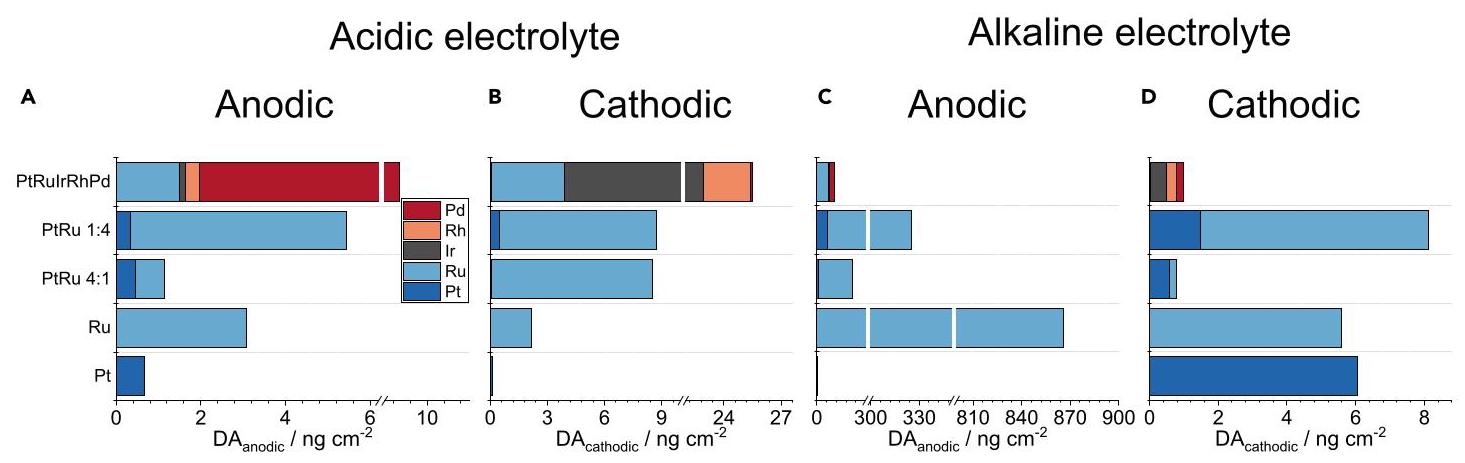
图6: (A-D)纯Pt、Ru、双金属PtRu(1:4和4:1元素比)以及PtRuIrRhPd HEA样品在(A,B)酸性(0.1 M HClO4电解质)和(C,D)碱性(0.05 M KOH电解质)条件下记录的阳极和阴极溶解特征计算得到的溶解量。
结果表明,通过调节相对稳定性较高的元素(此处为Pt)的含量,能够调节所得合金的稳定性。这表明只有一种或两种元素对给定的电催化反应有活性,而不是所有合金组成元素。