Ta-TiOx nanoparticles as radical scavengers to improve the durability of Fe-N-C oxygen reduction catalysts
Ta-TiOx纳米颗粒作为自由基清除剂提高Fe-N-C氧还原催化剂的耐久性
第一作者: Hua Xie1,7, Xiaohong Xie2,7
通讯作者: Guoxiang Hu3,5, Reza Shahbazian-Yassar5, Yuyan Shao2, Liangbing Hu1,2
1Department of Materials Science and Engineering, University of Maryland
2Pacific Northwest National Laboratory
3Department of Chemistry and Biochemistry, Queens College of the City University of New York
5Department of Mechanical and Industrial Engineering, University of Illinois at Chicago
DOI: 10.1038/s41560-022-00988-w |
期刊: Nature Energy |
年份: 2022
PDF原文
论文亮点
亮点 1: Ta-TiOx纳米颗粒作为高效自由基清除剂,能显著提高Fe-N-C氧还原催化剂的耐久性,通过主动清除·OH和HO₂·自由基以及分解H₂O₂。
亮点 2: 在质子交换膜燃料电池中,添加Ta-TiOx清除剂的催化剂在加速耐久性测试后电流密度衰减仅为3%,远低于未添加清除剂的33%,提供了一种主动防御策略。
研究背景
- 非贵金属催化剂(如Fe-N-C)对于降低质子交换膜燃料电池成本至关重要,但其在酸性环境中的耐久性差,性能在运行初期100小时内迅速衰减,限制工业应用。
- 耐久性问题主要源于氧化自由基(如·OH和HO₂·)的攻击,这些自由基由O₂的不完全还原通过H₂O₂形成,导致碳腐蚀、金属活性位点脱金属和氮基团质子化。
- 现有策略如提高碳基底石墨化或减少金属前体负载只能部分缓解降解,需要能主动直接消除H₂O₂和自由基的方法。
研究方法
- Ta-TiOx纳米颗粒合成: 使用高温脉冲技术,在氩气环境中通过焦耳加热(约1500 K,100 ms)和快速冷却(初始速率10^5 K/s)在Ketjenblack基底上均匀合成5 nm的Ta-TiOx纳米颗粒,形成金红石TaO₂相。
- 表征技术: 采用扫描电子显微镜(SEM)、透射电子显微镜(TEM)、高角度环形暗场扫描透射电子显微镜(HAADF-STEM)、X射线衍射(XRD)、氮气吸附-脱附等温线(BET法)和X射线光电子能谱(XPS)对纳米颗粒形貌、结构和组成进行表征。
- 自由基清除性能评估: 使用定制荧光光谱仪(以6-羧基荧光素为探针)和电子顺磁共振(EPR)自旋捕获技术(以DMPO为自旋陷阱)定量测定自由基清除效率。
- 电化学测试: 使用旋转环盘电极(RRDE)在O₂饱和的0.5 M H₂SO₄电解液中测试ORR活性和H₂O₂产率,进行循环伏安法耐久性测试(10,000次循环,0.6-1.0 V vs. RHE)。
- 燃料电池测试: 制备膜电极组件(MEA),在H₂/O₂和H₂/空气条件下进行加速耐久性测试(ADT),评估电压和功率密度极化曲线。
- 理论计算: 采用密度泛函理论(DFT)计算H₂O₂和自由基在TaO₂-OH表面的吸附能和反应路径,揭示清除机制。
主要结论
- Ta-TiOx纳米颗粒能高效清除·OH和HO₂·自由基并化学分解H₂O₂,显著提高Fe-N-C催化剂的耐久性,在RRDE测试中将H₂O₂产率降低51%(在0.7 V下)。
- 在加速耐久性测试中,添加Ta-TiOx清除剂的燃料电池在0.9 ViR-free下电流密度衰减仅为3%,而未添加清除剂的衰减为33%,证明其主动防御策略的有效性。
- DFT计算表明,TaO₂-OH表面对H₂O₂和自由基有强吸附能,并通过OH*和O*辅助路径高效分解H₂O₂为H₂O和O₂,揭示了清除机制的原子级细节。
图1: 有无Ta-TiOx清除剂时PGM-free催化剂在ORR过程中的耐久性示意图
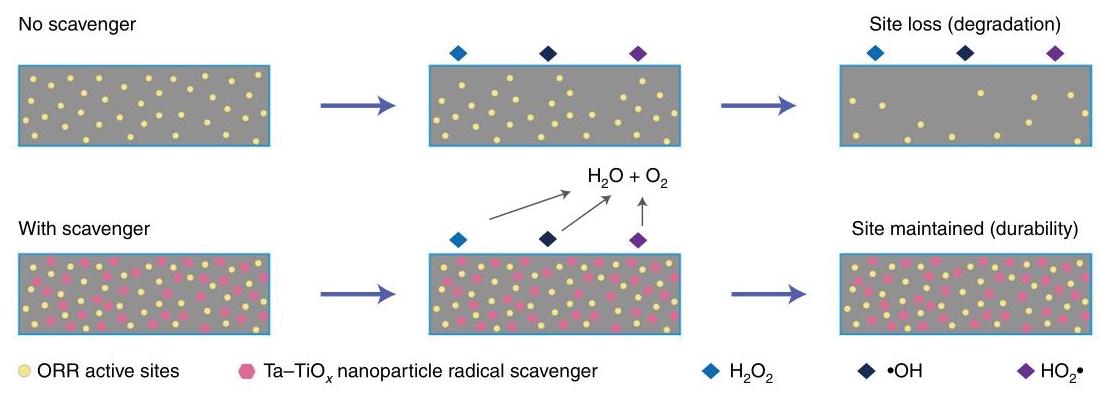
图1: 示意图比较有无Ta-TiOx/Ketjenblack清除剂时PGM-free催化剂的耐久性。无清除剂时,ORR性能因催化活性位点损失而快速衰减;引入Ta-TiOx清除剂后,能主动分解不完全氧还原路径中产生的·OH、HO₂·和H₂O₂。灰色背景为燃料电池中的催化剂涂层,ORR活性位点和Ta-TiOx纳米颗粒均匀分布在涂层中。
分析结果: 该图直观展示了Ta-TiOx清除剂的保护机制,通过主动清除自由基和H₂O₂,防止其对Fe-N-C活性位点的攻击,从而延长催化剂寿命。这种主动防御策略比传统的被动屏蔽更有效。
图2: Ta-TiOx自由基清除剂的形貌表征
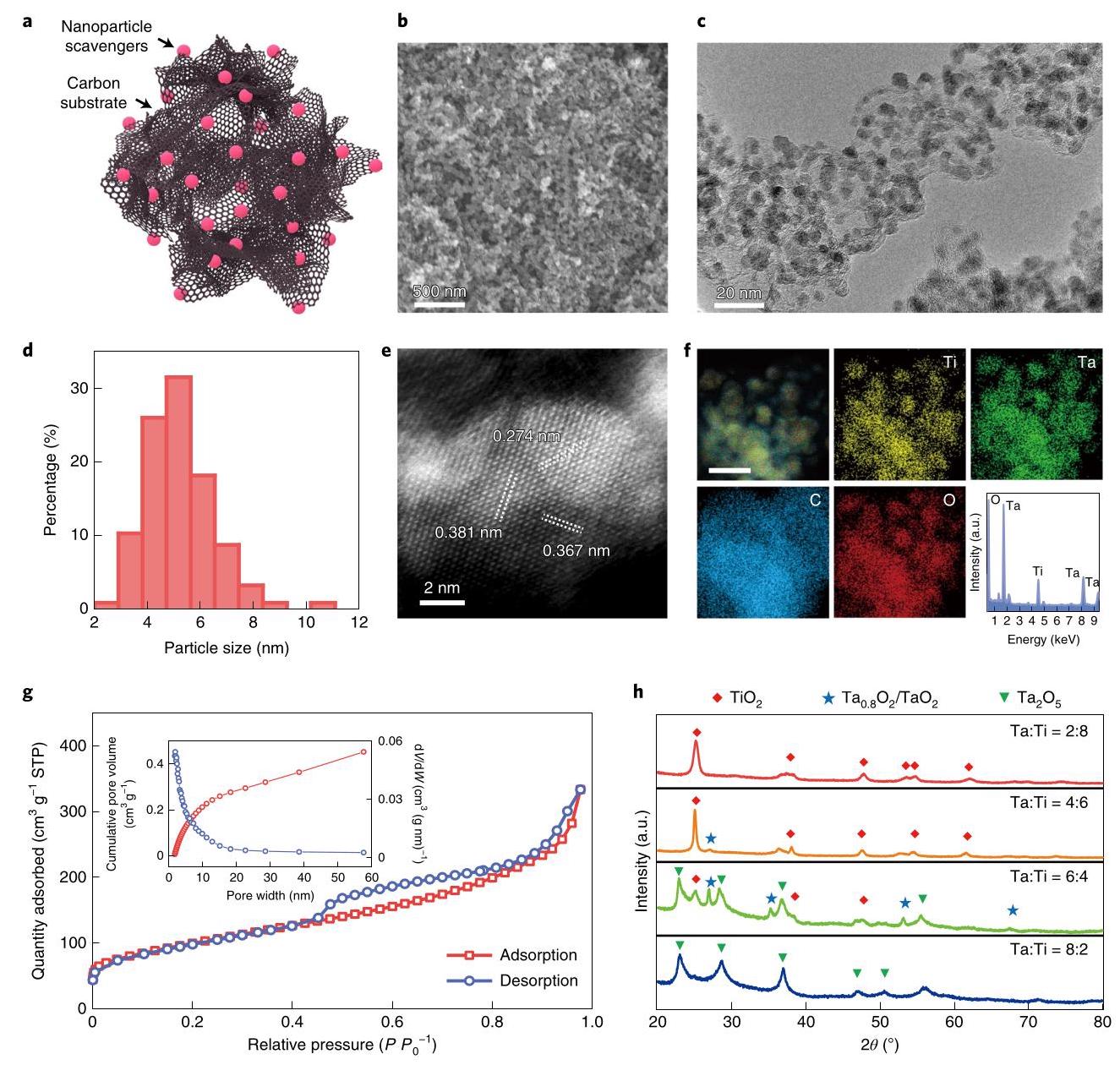
图2: Ta-TiOx自由基清除剂的形貌。(a) 示意图显示碳基底上分散良好的Ta-TiOx纳米颗粒作为清除剂。(b) Ta-TiOx纳米颗粒在KB上的SEM图像,显示材料的高孔隙率。(c) Ta-TiOx纳米颗粒的TEM图像,显示在基底上的均匀分散。(d) Ta-TiOx纳米颗粒的尺寸分布。(e) [001] zone axis下的HAADF-STEM图像,白色虚线表示晶格距离。(f) Ta-TiOx纳米颗粒的能量色散X射线光谱元素映射,显示两种氧化物的成功合金化。(g) KB负载的Ta-TiOx纳米颗粒在77 K下的N₂吸附-脱附等温线,插图为孔径分布。(h) Ta与Ti比例分别为2:8、4:6、6:4和8:2时合成的纳米颗粒的X射线衍射图谱,比例6:4时检测到金红石钽氧化物相。
分析结果: 合成方法成功制备了均匀分散的5.2±1.2 nm Ta-TiOx纳米颗粒,具有高孔隙率(BET表面积312.7 m²/g)和合金化结构。XRD显示在Ta:Ti=6:4时形成金红石TaO₂相,这与最高的H₂O₂清除能力相关,为后续性能测试提供了结构基础。
图3: Ta-TiOx/KB的自由基清除性能
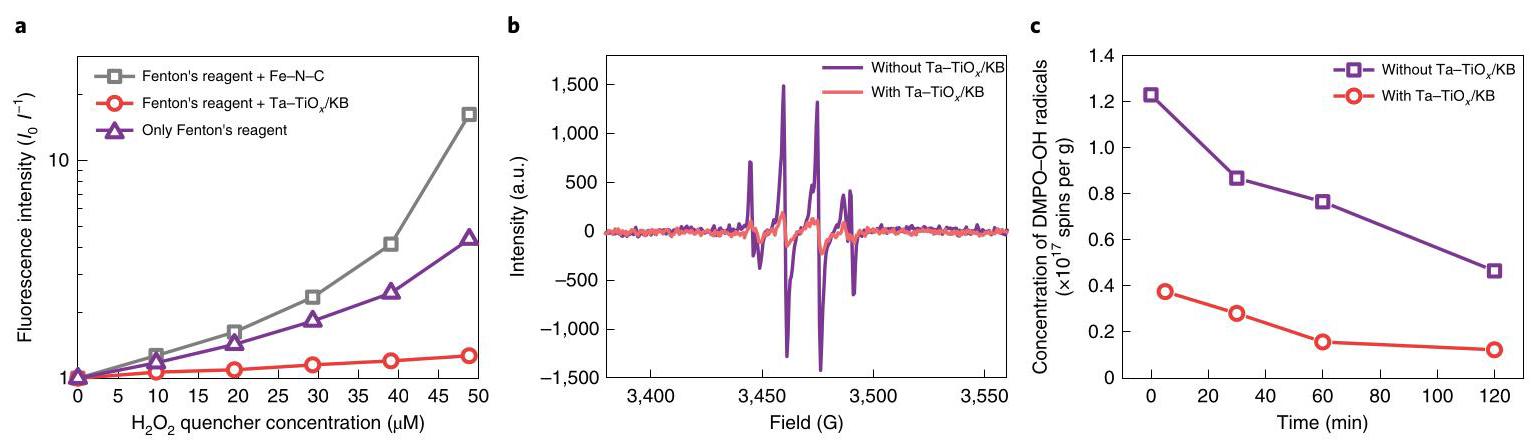
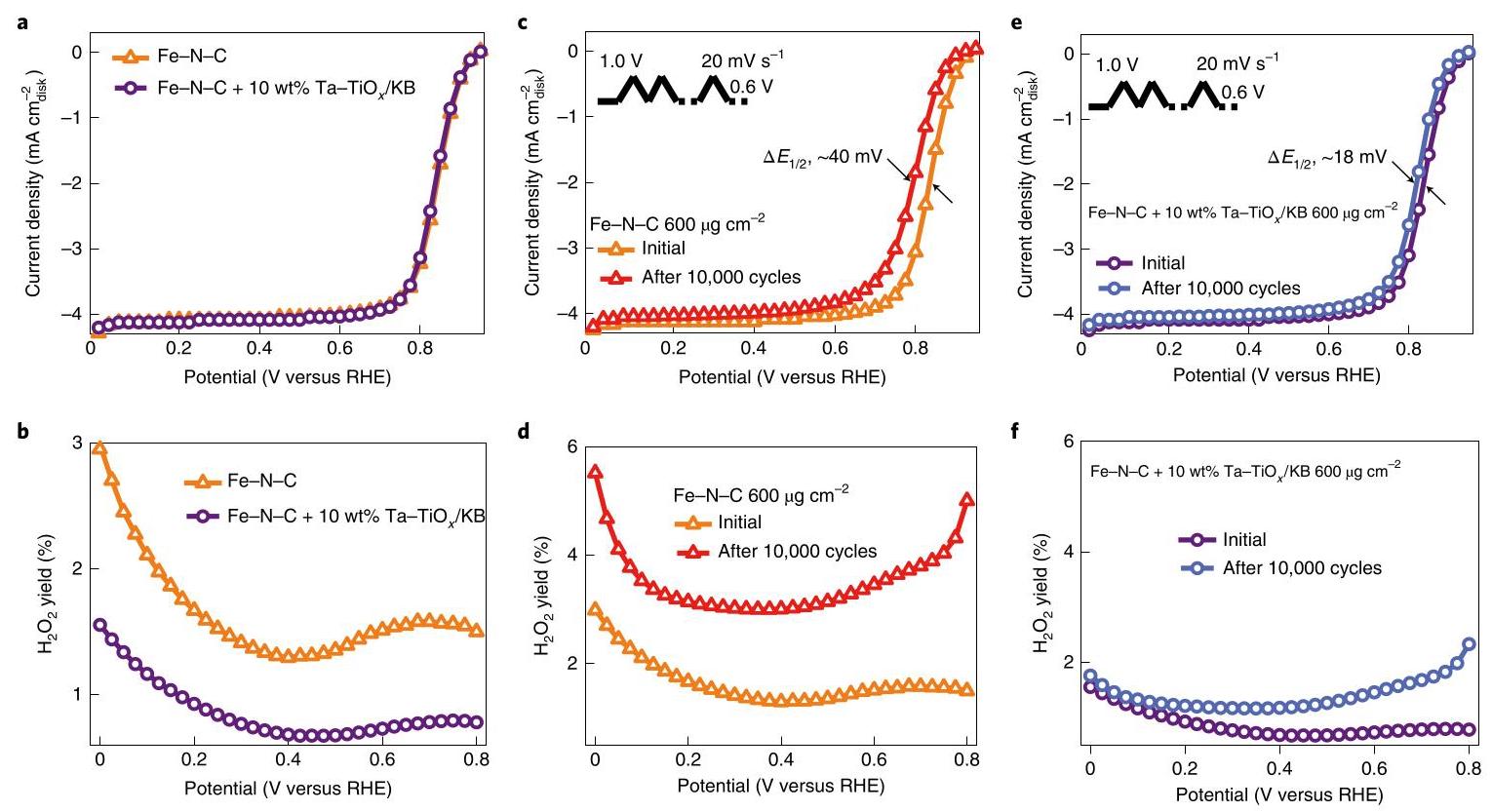
图3: Ta-TiOx/KB的自由基清除性能。(a) 使用6CFL染料在含Fenton试剂和Fe-N-C或Ta-TiOx清除剂的自由基溶液中获得的Stern-Volmer图,随H₂O₂/自由基淬灭剂浓度变化。(b) 添加和不添加Ta-TiOx/KB时OH-DMPO·自由基的电子顺磁共振谱。(c) 添加和不添加Ta-TiOx/KB时OH-DMPO·自由基浓度随时间衰减。
分析结果: 荧光光谱和EPR测试表明,Ta-TiOx/KB具有高效的自由基清除能力。Stern-Volmer图显示添加Ta-TiOx后荧光衰减显著降低,表明自由基被清除;EPR谱峰强度降低和OH-DMPO·浓度衰减动力学证实了其对·OH自由基的捕获作用,为后续电化学性能改进提供了依据。
图4: Ta-TiOx/KB清除剂对Fe-N-C催化剂的保护和H₂O₂抑制性能
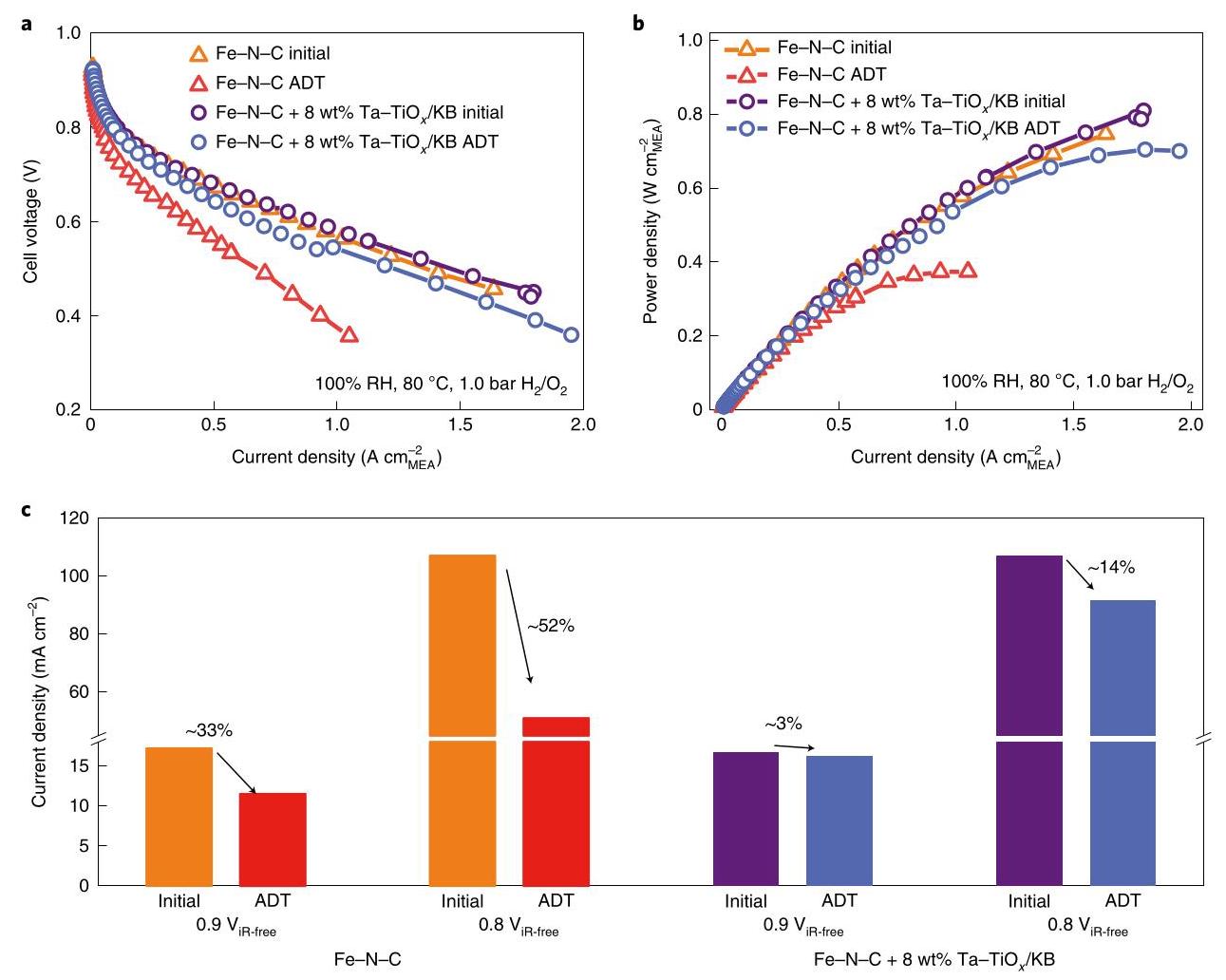
图4: Ta-TiOx/KB清除剂对Fe-N-C催化剂的保护和H₂O₂抑制性能。(a) 有无Ta-TiOx/KB清除剂(10 wt%,Ta:Ti=6:4)时Fe-N-C催化剂的ORR性能。(b) 有无清除剂时的H₂O₂产率。(c) 无清除剂时Fe-N-C催化剂的RRDE耐久性测试,显示初始循环和10,000次电位循环后的ORR性能。(d) 无清除剂时Fe-N-C催化剂在1和10,000次电位循环时的H₂O₂产率。(e) 有清除剂(10 wt%,Ta:Ti=6:4)时Fe-N-C催化剂的耐久性测试。(f) 有清除剂时Fe-N-C催化剂在1和10,000次电位循环时的H₂O₂产率。
分析结果: 添加Ta-TiOx/KB后,Fe-N-C催化剂的ORR活性保持稳定,H₂O₂产率显著降低(在0.7 V下从~1.6%降至0.88%)。耐久性测试显示,无清除剂时半波电位负移40 mV,H₂O₂产率增加2.4倍;而有清除剂时半波电位仅负移18 mV,H₂O₂产率保持低位,证明清除剂能连续快速去除生成的H₂O₂和自由基,保护活性位点。
图5: 有无Ta-TiOx/KB的PGM-free阴极的PEM燃料电池性能
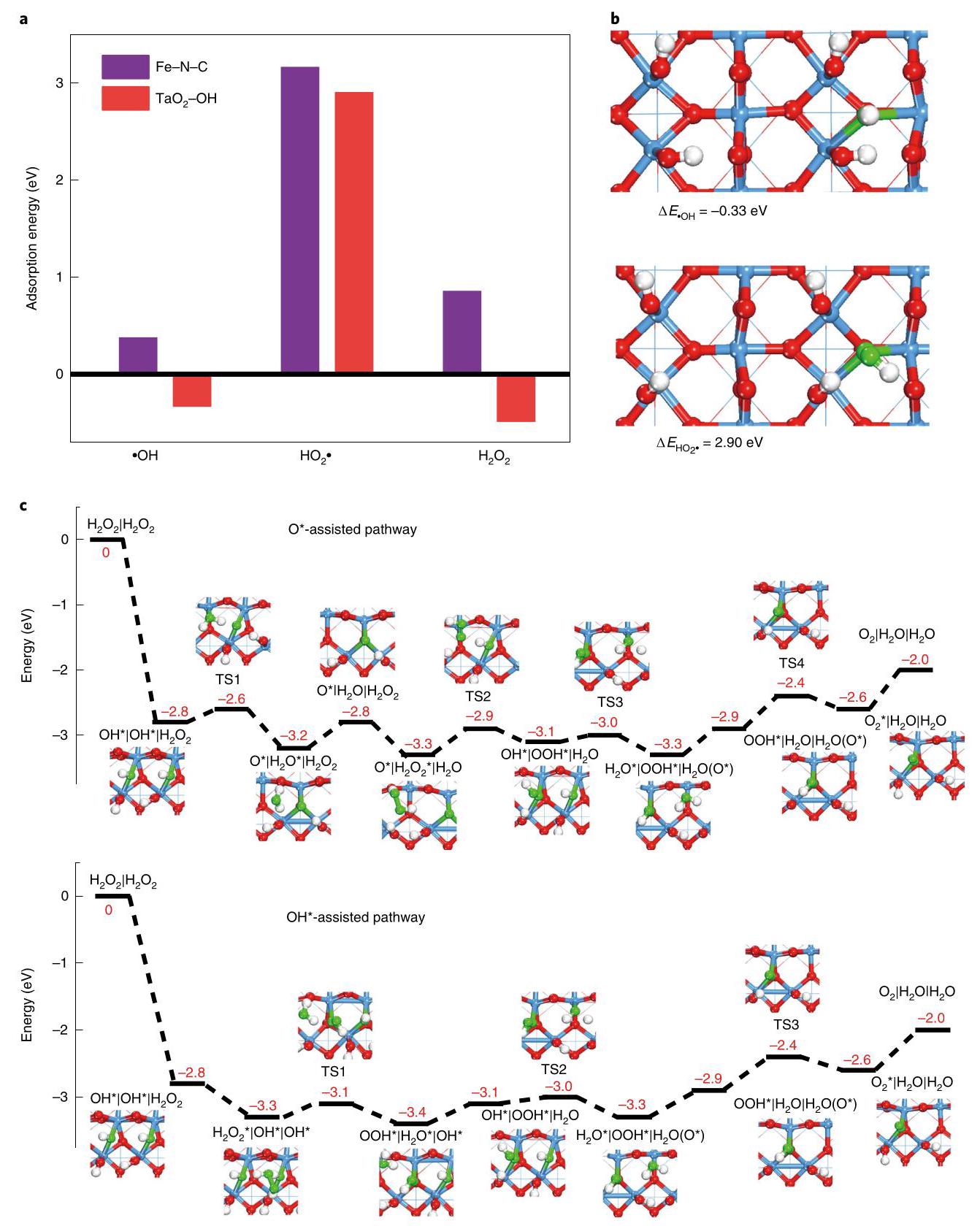
图5: 有无Ta-TiOx/KB的PGM-free阴极的PEM燃料电池性能。(a,b) ADT前后电池的电压(a)和功率密度极化(b)曲线。阴极Fe-N-C催化剂负载6.0 mg/cm²(有或无清除剂),阳极Pt/C负载0.2 mgPt/cm²。(c) ADT后有无Ta-TiOx/KB的电池电流密度衰减比较,Ta-TiOx清除剂显著提高燃料电池耐久性。
分析结果: 燃料电池测试显示,添加Ta-TiOx/KB清除剂的电池在ADT后性能衰减极小:在0.9 ViR-free下电流密度衰减仅3%,而未添加清除剂的衰减为33%。峰值功率达到700 mW/cm²,远高于未添加清除剂的370 mW/cm²,证实了清除剂在实际燃料电池环境中的有效性,提升了PGM-free阴极的耐久性。
图6: DFT计算理解Ta-TiOx/KB的自由基清除性能

图6: DFT计算理解Ta-TiOx/KB的自由基清除性能。(a) H₂O₂和相关自由基在Fe-N-C和TaO₂-OH表面的吸附能。(b) ·OH和HO₂·在TaO₂-OH(110)上的吸附结构和能量(ΔE)。(c) OH*和O*辅助路径去除H₂O₂和相关自由基的反应路径。
分析结果: DFT计算表明,TaO₂-OH(110)表面对H₂O₂、·OH和HO₂·的吸附能比Fe-N-C更强,能竞争性捕获自由基,防止其攻击活性位点。反应路径分析显示,OH*和O*辅助路径为H₂O₂分解提供 energetically efficient route,生成H₂O和O₂,解释了实验观察到的高效清除机制,为设计更佳清除剂提供了理论指导。







